Пролонгированные beta2-агонисты: место в терапии обструктивных болезней легких
Пролонгированные b2-агонисты при ХОБЛ
ХОБЛ включает в себя довольно неоднородную группу заболеваний, таких как хронический бронхит, эмфизему легких, заболевания малых дыхательных путей. Функциональные нарушения при ХОБЛ, в отличие от БА, фиксированные и лишь частично обратимы в ответ на терапию бронходилататорами и другими препаратами. Основными задачами терапии ХОБЛ являются не только улучшение функциональных легочных показателей, но и улучшение клинических симптомов, предотвращение развития обострений заболевания и улучшение качества жизни больных. Бронходилататоры являются основными средствами длительной терапии ХОБЛ, препаратами первой линии являются антихолинергические препараты, кроме того, большое значение имеют также симпатомиметики и теофиллины. Пролонгированные b2-агонисты являются относительно новым классом препаратов терапии ХОБЛ, однако результаты исследований, проведенных в последнее время, показали высокую эффективность данных препаратов при их постоянном приеме, что возможно в скором времени может поставить их в ранг препаратов первой линии длительной терапии ХОБЛ.
Влияние пролонгированных b2-агонистов на клинические симптомы и функциональные показатели
Бронходилатирующий эффект сальметерола и формотерола у больных ХОБЛ был показан во многих краткосрочных исследованиях: выраженность эффекта сравнима с b2-агонистами короткого действия, однако продолжительность эффекта значительно дольше.
Два крупных многоцентровых рандомизированных контролируемых исследования, посвященных изучению эффективности пролонгированных b2-агонистов, проведены в Европе и Северной Америке. В Европейское исследование были включены 674 больных ХОБЛ (средний возраст 62 года, средний ОФВ1 – 1,31 л), разделены на 3 группы, одна из которых получала сальметерол 50 мкг 2 раза сутки, вторая – сальметерол 100 мкг 2 раза в сутки, и третья – плацебо; терапию проводили в течение 16 нед. В ходе терапии у больных, принимавших сальметерол, наблюдали достоверное улучшение дневных симптомов и снижение приема сальбутамола в течение дня. Функциональные легочные показатели также улучшились при терапии сальметеролом (до 7%), на протяжении периода исследования дистанция в тесте с 6-минутной ходьбой достоверно не различалась между группами, однако диспноэ в конце теста было ниже у больных, принимавших сальметерол 50 мкг 2 раза в сутки через 8 нед (p = 0,024) и через 16 нед (p = 0,004) терапии. Число побочных эффектов было приблизительно одинаковым во всех группах, за исключением тремора, который был более выражен у больных, принимавших сальметерол в дозе 100 мкг 2 раза в день (p = 0,005).
В Североамериканское исследование были включены 411 больных ХОБЛ (средний ОФВ1 1,3 л, средний возраст 63 года), все пациенты были разделены на три группы и в течение 12 нед принимали либо сальметерол 42 мкг (= 50 мкг в Европе) 2 раза в сутки, либо ипратропиум 36 мкг (= 40 мкг в Европе) 4 раза в сутки, либо плацебо. Значительное улучшение показателя ОФВ1 наблюдалось у больных, принимавших сальметерол, причем на 4-й и 8-й неделях исследования прирост ОФВ1 был даже выше, чем у больных в группе ипратропиума (p < 0,005). Сальметерол также оказался более эффективным препаратом по сравнению с ипратропиумом по влиянию на ночные симптомы заболевания (p = 0,043). Одной из основных конечных точек данного исследования являлось изучение влияния препаратов на диспноэ – кардинальный симптом ХОБЛ. Было показано, что и сальметерол, и ипратропиум позволяют достоверно уменьшить выраженность диспное в течение всего срока терапии. По числу побочных эффектов все три группы больных не различались между собой. В течение 12 нед терапии не было отмечено развития толерантности к сальметеролу.
Традиционные функциональные показатели (ОФВ1, ПОС) при ХОБЛ часто не позволяют оценить положительный ответ больных на бронходилататоры. Спирометрические тесты являются форсированными маневрами и усиливают ранний коллапс дыхательных путей, что не позволяет судить об изменении бронхиальной обструкции периферических дыхательных путей. В такой ситуации, как ХОБЛ, более подходящими исследованиями могут быть тесты, не требующие форсированного маневра, например, оценка бронхиального сопротивления. В исследовании B.Maesen для оценки бронходилатирующего эффекта формотерола у больных ХОБЛ были использованы неспирометрические показатели: бронхиальное сопротивление и работа дыхания. Изучались дозы формотерола 6 и 24 мкг, ингалируемые через турбухалер и плацебо у 12 больных в течение 3 последовательных дней. Обе дозы препарата уже через 10 мин после ингаляции приводили к выраженному снижению бронхиального сопротивления (на 21–25%, p = 0,003 по сравнению с плацебо) и уменьшению работы дыхания (на 28–30%, p = 0,0007 по сравнению с плацебо), положительный эффект формотерола продолжался не менее 12 ч. Интересно отметить, что несмотря на выраженные изменения бронхиального сопротивления, изменения ОФВ1 составили лишь 7 ± 4% (в ответ на 24 мкг формотерола).
Таблица 2. Сравнение b2-агонистов короткого и длительного действия (Global Initiative for Asthma (CINA). WHO/NHLBI, 1998)
| b2-агонисты короткого действия(препараты для облегчения симптомов) | Пролонгированные b2-агонисты (длительная превентивная терапия) |
| Быстрое действие, приводящее к разрешению бронхоконстрикции острых симптомов- одышки, кашля, заложенности в грудной клетке | Используются ежедневно на постоянной основе для достижения и поддержания контроля персистирующей астмы |
| Короткая продолжительность действия (4–6 ч) | Длительная продолжительность действия (как минимум 12 ч) |
| Быстрое начало действия (1–3 мин) | Быстрое начало действия (1–3 мин, формотерол) или относительно медленное (10–20 мин, сальметерол) |
| Предотвращение развития постнагрузочного бронхоспазма | Предотвращение развития постнагрузочного бронхоспазма |
Рис. 2. Механизм действия b2-агонистов (GP. Anderson Life Sci, 1993)
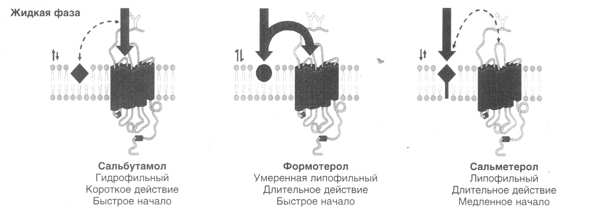
Рис. 3. Сравнение начала действия формотерола, сальметерола и сальбутамола (J.A. van Noord и соавт. Eur Respir J, 1996).
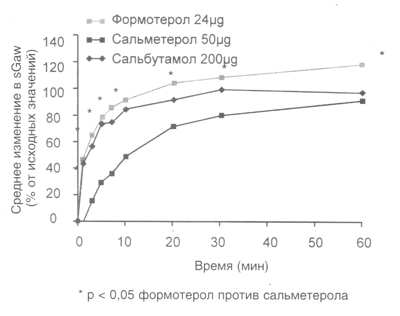
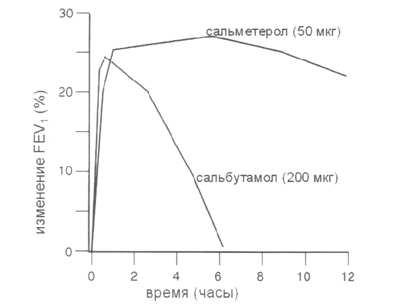
Рис. 4. Сравнение продолжительности действия сальметерола и сальбутамола (P.J.Barnes, S. Godfrey; Asthma Therapy, 1998).
Влияние пролонгированных b2-агонистов на качество жизни больных ХОБЛ
Пролонгированные b2-агонисты, независимо от изменений функциональных легочных показателей, значительно улучшают клинические симптомы и качество жизни больных ХОБЛ. В исследовании P.Jones и соавт., включавшем 283 больных ХОБЛ, терапия сальметеролом в дозе 50 мкг 2 раза в сутки приводила к значительному улучшению качества жизни, оцененного по анкете Святого Георгия. Увеличение дозы сальметерола до 100 мкг дважды в сутки не приводило к дальнейшему улучшению клинических симптомов и функциональных показателей, в то время как качество жизни было достоверно ниже по сравнению с дозой 50 мкг 2 раза в сутки, что, вероятно, отражает большее число побочных реакций (тремор) при использовании большей дозы препарата.
Значительное улучшение качества жизни на фоне приема формотерола, было показано в многоцентровом Европейском исследовании, включавшем 780 больных ХОБЛ. Повышение числа баллов качества жизни, также оцененное по анкете Святого Георгия, наблюдали у больных, принимавших формотерол в дозах 12 и 24 мкг дважды в день (p < 0,001 и p< 0,01 соответственно по сравнению с плацебо), качество жизни при приеме формотерола в дозах 12 мкг 2 раза в день было выше, чем при приеме ипратропиума 40 мкг 4 раза в сутки (p < 0,005). Улучшение числа баллов по анкете качества жизни наблюдали также и у больных с необратимой бронхиальной обструкцией.
Влияние пролонгированных b2-агонистов на частоту развития обострений ХОБЛ
Основной задачей длительной терапии ХОБЛ является снижение числа обострений заболевания. Важнейшим результатом исследования D.Mahler и соавт. явилось полученное доказательство увеличения времени между обострениями ХОБЛ при приеме сальметерола по сравнению с плацебо (p = 0,0052) и ипратропиума (p = 0,041). Во время 12-недельного периода исследования обострения ХОБЛ реже возникали у больных, принимавших сальметерол (20,7% больных), по сравнению с больными групп ипратропиума и плацебо (30,8 и 32,9% пациентов соответственно).
Недавно в многоцентровом Европейском исследовании, включавшем 780 больных ХОБЛ, было показано, что число "плохих дней" во время терапии формотеролом в дозе 12 мкг 2 раза в день в течение 12 нед было значительно меньше, чем у больных, принимавших ипратропиум 40 мкг 4 раза в сутки или плацебо .
Одним из возможных объяснений снижения числа обострений ХОБЛ при приеме сальметерола может являться показанная in vitro способность препарата защищать респираторный эпителий от повреждения, вызываемого бактериальными токсинами. При ХОБЛ бактериальная инфекция носит хронический характер и может вызывать обострения, являясь таким образом ведущим фактором, определяющим прогрессирование болезни. Согласно гипотезе "порочного круга" присутствие бактерий вызывает нарушение защитных механизмов респираторного тракта. Эти изменения предрасполагают к дальнейшему развитию инфекций, замыкая "порочный круг". Бактериальные продукты и протеазы воспалительных клеток повреждают респираторный эпителий, ингибируют его цилиарную активность, что обеспечивает оптимальные условия для бактериальной колонизации.
В двух последовательных экспериментальных исследованиях R.Dowling и соавт. получили данные о способности сальметерола обеспечивать защиту эпителиальных клеток дыхательных клеток от микроорганизма Pseudomonas aeruginosa и его продуктов агрессии – пиоцианина и эластазы, а также от другого микроорганизма – Haemophilus influenzae. Если данные наблюдения in vitro можно экстраполировать на больных ХОБЛ, то можно предположить, что пролонгированные b2-агонисты способны снижать число обострений заболевания, вмешиваясь в "порочный круг" ХОБЛ.
Сочетание пролонгированных b2-агонистов с другими препаратами при ХОБЛ
Во всех приведенных выше исследованиях при ХОБЛ оценивались эффекты монотерапии пролонгированными b2-агонистами, об эффективности сочетанной терапии сальметерола или формотерола с другими препаратами при ХОБЛ известно гораздо меньше.
В настоящее время доказано, что сочетанная терапия b2-агонистами короткого действия и ипратропиумом более эффективна при длительной терапии ХОБЛ, чем монотерапия каждым из этих препаратов. Первые данные об эффективности комбинации сальметерола и ипратропиума получены в многоцентровом рандомизированном контролированном голландском исследовании, включавшем 144 больных ХОБЛ (возраст 64 ± 7 лет, ОФВ1 44 ± 11%). В исследовании в течение 12 нед сравнивали три режима терапии: 1) сочетание сальметерола 100 мкг/сут и ипратропиума 160 мкг/сут; 2)монотерапия сальметеролом 100 мкг/сут и 3)плацебо. В группах активной терапии наблюдали улучшение клинических симптомов, утренних показателей ПОС (p < 0,001) и снижение потребности в коротких b2-агонистах. Однако улучшение показателей ОФВ1 и проходимости дыхательных путей (sGaw) было больше выражено при приеме сочетанной терапии по сравнению с монотерапией сальметеролом (7 и 11% для ОФВ1, 60 и 94% для sGaw соответственно). Число обострений ХОБЛ на протяжении периода исследования было достоверно ниже только в группе сочетанной терапии (13% против 36% в группе плацебо, p < 0,01); группа больных, получавших монотерапию сальметеролом, занимала промежуточное место по числу обострений (23%). Число побочных эффектов было невелико и различалось между группами. Таким образом, сочетание антихолинергических препаратов и пролонгированных b2-агонистов может приносить дополнительный эффект при терапии больных ХОБЛ.
В отличие от БА сочетанная терапия ИКС и пролонгированными b2-агонистами также практически не изучена при ХОБЛ. В 3-месячном рандомизированном контролируемом исследовании M.Cazzola и соавт. показали, что наибольшее улучшение функциональных показателей наблюдалось у больных, получавших терапию сальметеролом 100 мкг/сут и флютиказоном 1000 мкг/сут (прирост ОФВ1 0,24 л) по сравнению с монотерапией сальметеролом 100 мкг/сут (прирост ОФВ1 0,16 л). Учитывая возможность ИКС и пролонгированных b2-агонистов снижать число обострений ХОБЛ, нельзя исключить, что сочетанная терапия данными препаратами приведет к большему эффекту, чем монотерапия каждым из них.
www.consilium-medicum.com /Том 3/N 3 (2001).
Литература
1. Moore RH, Khan A, Dickey BF Long-acting inhaled b2-agonists in asthma therapy. Cheat 1998; 113: 1095-108.
2. Anderson GP Long acting inhaled beta-adrenoceptor agonists: the comparative pharmacology of formoterol and salmeterol. Agents Actions Suppl 1993; 43: 253-69.
3. Anderson GP, Linden A, Rabe KF Why are long-acting beta-adrenoceptor agonists long-acting? Eur Respir J 1994; 7: 569-78.
4. Lotvall J Pharmacology of bronchodilators used in the treatment of COPD. Respir Med 2000; 94 (Suppl.E): S6-S10.
5. Palmqvist M, Persson G, Lazer L, Rosenborg J, Larsson P, Lotvall J Inhaled dry-power formoterol and salmeterol in asthmatic patients: onset of action, duration of effect and potency. Eur Respir J 1997; 10: 2482-9.
6. Anderson P, Lotvall J, Linden A Relaxation kinetics of formoterol and salmeterol in the guinea pig trachea in vitro. Lung 1996; 174: 159-70.
7. Palmqvist M, Ibsen T, Mellen A, Lotvall J Comparison of relative efficacy of formoterol and salmeterol in asthmatic patients. Am J Respir Crit Care Med 1999; 160: 244-9.
8. Totterman KJ, Huhti L, Sutinen E et al. Tolerability to high doses of formoterol and terbutaline via Turbuhaler for 3 days in stable asthmatic patients. Eur Respir J 1998; 12: 573-9.
9. Korosec M, Novak RD, Myers E et al. Salmeterol does not compromise the bronchodilator response to albuterol during acute episodes of asthma. Am J Med 1999; 107: 209-13.
10. Pearlman DS, Chervinsky P, LaForce C et al. A comparison of salmeterol with albuterol in the treatment of mild-to-moderate asthma. N Engl J Med 1992; 327: 1420-5.
11. D'Alonzo GE, Nathan RA, Henochowicz S et al. Salmeterol xinafoate as maintenance therapy compared with albuterol in patients with asthma. JAMA 1994; 271: 1412-6.
12. Boulet LP, Laviolette M, Boucher S et al. A 12-week comparison of salmeterol and salbutamol in the treatment of mild-to-moderate asthma: a Canadian multicenter study. J Allergy Clin Immunol 1997; 99: 13-21.
13. Britton MG, Earnshaw JS, Palmer JB. A 12-month comparison of salmeterol with salbutamol in asthmatic patients: European Study Group. Eur Respir J 1992; 5: 1062-7.
14. Hekking PR, Maesen FPV, Greefhorst A et al. Long-term efficacy of formoterol compared to salbutamol. Lung 1990; 168 (Suppl): 76-82.
15. Kesten S, Chapman KR, Broder I et al. A 3-month comparison of twice daily inhaled formoterol vs four times daily inhaled albuterol in the management of stable asthma. Am Rev Respir Dis 1991; 144: 622-5.
16. Kesten S, Chapman KR, Broder I et al. Sustained improvement in asthma with long-term use of formoterol fumarate. Ann Allergy 1992; 69: 415-20.
17. Kemp JP, Cook DA, Incaudo GA, Corren J, Kalberg C, Emmett A, Cox FM, Rickard K Salmeterol improves quality of life in patients with asthma requiring inhaled corticosteroids. Salmeterol Quality of Life Study Group. J Allergy Clin Immunol 1998; 101: 188-95.
18. Juniper EF, Johnston PR, Borkhoff CM, et al. Quality of life in asthma clinical trials: comparison of salmeterol and salbutamol. Am J Respir Crit Care Med 1995; 151: 66-70.
19. Turner-Warwick M. Epidemiology of nocturnal asthma. Am J Med 1988; 85: 6-8.
20. Kraft M, Wenzel SE, Bettinger CM et al. The effect of salmeterol on nocturnal symptoms, airway function, and inflammation in asthma. Chest 1997; 111: 1249-54.
21. Brambilla C, Chastang C, Georges D et al. Salmeterol compared with slow-release terbutaline in nocturnal asthma. Allergy 1994; 49: 421-6.
22. Fitzpatrick MF, Mackay T, Driver H et al. Salmeterol in nocturnal asthma; a double blind, placebo controlled trial of a long acting inhaled b2 agonist. BMJ 1990; 301: 1365-8.
23. Anderson SD, Rodwell LT, Du Toit J et al. Duration of protection by inhaled salmeterol in exercise-induced asthma. Chest 1991; 100: 1254-60.
24. Kemp JP, Dockhorn RJ, Busse WW et al. Prolonged effect of inhaled salmeterol against exercise-induced bronchospasm. Am J Respir Crit Care Med 1994; 150: 1612-5.
25. Henriksen JM, Agertoft L, Pedersen S Protective effect and duration of action of inhaled formoterol and salbutamol on exercise induced asthma in children. J Allergy Clin Immunol 1992; 89: 1176-82.
26. Ramage L, Cree IA, Dhillon DP. Comparison of salmeterol with placebo in mild asthma: effect on peripheral blood phagocyte function and cytokine levels. Int Arch Allergy Immunol 1994; 105: 181-4.
27. National Asthma Education Program and Prevention Program Expert Panel Report II. Guidelines for the diagnosis and management of asthma. Bethesda, Md: NHLBI, NIH, 1997.
28. Chung KF. The complementary role of glucocorticosteroids and long-acting beta-adrenergic agonists. Allergy 1998; 53 (Suppl.42): 7-13.
29. Greening AP, Ind PW, Northfield M et al. Added salmeterol versus higher-dose corticosteroid in asthma patients with symptoms on existing inhaled corticosteroid: Allen & Hanburys Limited UK Study Group. Lancet 1994; 344: 219-24.
30. Woolcock A, Lundback B, Ringdal N et al. Comparison of addition of salmeterol to inhaled steroids with doubling of the dose of inhaled steroids. Am J Respir Crit Care Med 1996; 153: 1481-8.
31. Devoy MAB, Fuller RW, Palmer JBD Are there any detrimental effects of the use of inhaled long-acting beta2 -agonists in the treatment of asthma? Chest 1995; 107: 1116-24.
32. Shrewsbury S, Pyke S, Britton M Meta-analysis of increased dose of inhaled steroid or addiction of salmeterol in symptomatic asthma (MIASMA). Brit Med J 2000; 320: 1368-73.
33. Pauwels RA, Lofdahl CG, Postma DS, et al. Effect of inhaled formoterol and budesonide on exacerbations of asthma. N Engl J Med 1997; 337: 1405-11.
34. Sue-Chu M, Wallin A, Wilson S, Ward T, Sandstrom T, Djukanovic R, Holgate ST, Bjermer L Bronchial biopsy study in asthmatics treated with low and high dose fluticasone propionate (FP) compared to low dose FP combined with salmeterol. Eur Respir J 1999; 14 (Suppl.): 124s.
35. Чучалин А.Г., Калманова Е.Н., Айсанов З.Р., Стулова О.Ю., Беда М.В. Применение фиксированных комбинаций ингаляционных кортикостероидов и длительно действующих b2-агонистов в лечении бронхиальной астмы. Пульмонология 2000; 1: 81-5.
36. Zetterstrom O, Buhl R, Mellen H et al. The single inhaler product containing both budesonide/formoterol improves asthma control in adults. Eur Respir J 2000; 16 (Suppl.31): 455s.
37. Kavuru M, Melamed J, Gross G et al. Salmeterol and fluticasone propionate combined in a new powder inhalation device for the treatment of asthma: a randomised, double blind placebo controlled trial. J Allergy Clin Immunol 2000; 105: 1108-16.
38. Lanes SF, Lee L, Wentworth CE Risk of emergency care, hospitalization, and ICU stays for acute asthma among recipients of salmeterol. Am J Respir Crit Care Med 1998; 158: 857-61.
39. Beasley R, Pearce N, Crane J, et al. Beta-agonists: what is the evidence that their use increases the risk of asthma morbidity and mortality? J Allergy Clin Immunol 1999; 103: S18-S30.
40. European Respiratory Society. Optimal assessment and management of chronic obstructive pulmonary disease (COPD). Eur.Respir. J. 1995; 8: 1398-420.
41. Cazzola M, Matera MG Should long-acting b2 -agonists be considered an alternative first choice option for the treatment of stable COPD? Respir Med 1999; 93: 227-9.
42. Ramirez-Venegas A, Ward J, Lentine T et al. Salmeterol reduces dyspnea and improves lung function in patients with COPD. Chest 1997; 112: 336-40.
43. Boyd G, Morice AH, Pounsford JC et al. An evaluation of salmeterol the treatment of chronic obstructive pulmonary disease (COPD). Eur Respir J 1997; 10: 815-21.
44. Mahler DA, Donohue JF, Barbee RA et al. Efficacy of salmeterol xinafoate in the treatment of COPD. Chest 1999; 115: 957-65.
45. Maesen BLP, Westermann CJJ, Duurkens VAM, van den Bosch JMM Effects of formoterol in apparently poorly reversible chronic obstructive pulmonary disease. Eur Respir Dis 1999; 13: 1103-8.
46. Jones PW, Bosh TK. Quality of life changes in COPD patients treated with salmeterol. Am J Respir Crit Care Med 1997; 155: 1283-9.
47. Greefhorst APM, Dahl R, Nowak D et al. Formoterol dry powder improves the quality of life of patients with COPD whereas the effect of ipratropium is similar to placebo. Eur Respir J 2000; 16 (Suppl.31): 51s.
48. Greefhorst APM, Dahl R, Nowak D et al. Effect of inhaled formoterol and ipratropium bromide on quality of life, "bad days" and exacerbations in patients with COPD. Am J Respir Crit Care Med 2000; 161: A490.
49. Dowling RB, Rayner CFJ, Rutman A et al. Effect of salmeterol on Pseudomonas aeruginosa infection of respiratory mucosa. Am J Respir Crit Care Med 1997; 155: 327-36.
50. Dowling RB, Johnson M, Cole PJ, Wilson R Effect of salmeterol on Haemophilus influenzae infection of respiratory mucosa in vitro. Eur Respir J 1998; 11: 86-90.
51. Combivent Inhalational Aerosol Study Group. In chronic obstructive pulmonary disease, a combination of ipratropium and albuterol is more effective than either agent alone: an 85-day multicenter trial. Chest 1994; 105: 1411-9.
52. van Noord JA, de Munck DR, Bantje TA, Hop WC, Akveld ML, Bommer AM Long-term treatment of chronic obstructive pulmonary disease with salmeterol and the additive effect of ipratropium. Eur Respir J 2000; 15: 878-85.
53. Cazzola M, Di Lorenzo G, Di Perna F, Calderaro F, Testi R, Centanni S Additive effects of salmeterol and fluticasone or theophylline in COPD. Chest 2000; 118: 1576-81.
54. Nathan R, Seltzer JM, Kemp JP et al. Safety of salmeterol in the maintenance treatment of asthma. Ann Allergy Asthma Immunol 1995; 75: 243-8.
55. Smyth ET, Pavord ID, Wong CS et al. Interaction and dose equivalence of salbutamol and salmeterol in patients with asthma. BMJ 1993; 306: 543-5.
56. Martin RM, Dunn NR, Freemantle SN, Mann RD Risk of non-fatal cardiac failure and ischaemic heart disease with long acting b2 agonists. Thorax 1998; 53: 558-62.
57. D’Amato M, Di Perna F, Califano C, Calderano F, Cazzola M Formoterol Turbuhaler as a rescue medication in patients with acute exacerbations of partially reversible COPD. Eur Respir J 2000; 16 (Suppl.31): 275s.
58. Berggren F, Ekstrom T, Berggren F. Cost-utility analysis of formoterol (Oxis“) and terbutaline (Brycanyl“) used as needed in patients with moderate asthma. Eur Respir J 2000; 16(Suppl.31): 315s
59. Cazzola M, Imperatore F, Salzillo A et al. Cardiac effects of formoterol and salmeterol in patients suffering from COPD with preexisting cardiac arrhythmias and hypoxemia. Chest 1998; 114: 411-5.
60. Dahl R, Kristufek P, Greefhorst APM et al. The cardiac safety profile of formoterol dry powder is similar to placebo in patients with COPD. Eur Respir J 2000; 16 (Suppl.31): 51s.


Ваш комментарий