Эхокардиографические показатели систолической и диастолической функций левого желудочка при ишемической кардиомиопатии
Ключевые слова: ишемическая кардиомиопатия, эхокардиография, систола, диастола
Ишемическая кардиомиопатия (ИКМП) характеризуется дилатацией прежде всего левого желудочка (ЛЖ), а в поздних стадиях – и других камер сердца, прогрессированием сердечной недостаточности (СН) по типу систолической и диастолической дисфункции, появлением локальных зон асинергии. Нарушение насосной функции ЛЖ при ИКМП обусловлено наличием как мелких диффузных очагов заместительного склероза и интерстициального фиброза, возникших вследствие стенозирующего атеросклероза венечных артерий, так и крупных очагов рубцовых изменений после перенесенного инфаркта миокарда (ИМ). ИКМП – это типичное проявление дезадаптивного ремоделирования ЛЖ вследствие замещения значительной части погибших кардиомиоцитов фиброзной тканью, изменения взаиморасположения интактных миоцитов. Как правило, при ИКМП ремоделирование ЛЖ происходит медленно, в течение длительного времени, при этом включаются долгосрочные компенсаторные механизмы, постепенно увеличиваются камеры сердца, изменяется их геометрическая форма [5, 10, 15]. В начальных стадиях ИКМП нарушение насосной функции миокарда преходяще и обусловлено его ишемией. По мере прогрессирования коронарного атеросклероза СН становится стойкой. Обычно она прогрессирует медленно, вначале протекает по левожелудочковому типу и лишь в поздних стадиях становится бивентрикулярной. У некоторых больных с острым трансмуральным ИМ при прогрессивном дезадаптивном ремоделировании происходит быстрое (в течение 3–6 мес) расширение полости ЛЖ, снижается его сократительная способность, формируется ИКМП [4, 8, 9].
У больных с ИКМП часто выявляют локальные зоны акинезии и дискинезии с наличием демаркационной линии, утолщение стенки венечных артерий и атеросклеротические бляшки в них [1]. Распространенная дискинезия ЛЖ, охватывающая два его соседних сегмента и более выявлена у 50% больных с ИКМП и лишь у 10% – с идиопатической дилатационной кардиомиопатией (КМП) [6]. При возникновении застойной СН отмечают значительные нарушения внутрисердечной гемодинамики. Точное определение параметров систолической и диастолической функций ЛЖ позволяет выбрать оптимальный вариант лечения [12, 14]. Работы, посвященные ИКМП, немногочисленны, чаще всего о ней упоминают в разделах дифференциальной диагностики идиопатической дилатационной КМП и других заболеваний, при которых выявляют дилатацию ЛЖ и застойную СН. Эхокардиографические параметры внутрисердечной гемодинамики тесно коррелируют с таковыми, полученными при ангиографии.
Цель исследования – всесторонняя эхокардиографическая характеристика систолической и диастолической функций ЛЖ при ИКМП различной степени тяжести.
Материал и методы
Под наблюдением находились 103 больных с ИКМП в возрасте от 42 до 67 лет, в среднем (53,0±4,8) года. Мужчин было 84 (81,6%), женщин – 19 (18,4%). У 76 больных в анамнезе были указания на 1–3 документированных ИМ, у 27 – таких указаний не было. При тщательном клиническом и инструментальном исследовании у 15 больных обнаружены признаки рубцовых изменений различной локализации. У 12 пациентов ишемическую болезнь сердца (ИБС) диагностировали на основании данных клинических исследований и результатов коронарографии. У всех больных выявлена хроническая СН, в том числе II функционального класса (ФК) по NYHA – у 43 (41,7%), III ФК – у 48 (46,6%), IV ФК – у 12 (11,7%). Больных с ревматическими и врожденными пороками сердца, существенной миксоматозной дегенерацией митрального клапана в исследование не включали.
Эхокардиография проведена с использованием аппаратов Sonos-100 (Hewlett Packard, США), Versa (Siemens, Германия) по общепринятой методике [11]. В двухмерном режиме определяли конечно-диастолический (КДО) и конечно-систолический (КСО) объем, ударный объем (УО), фракцию выброса (ФВ), массу миокарда (ММ) ЛЖ, индекс КДО/ММ и индекс локальной сократимости (ИЛС). В М-режиме измеряли конечно-диастолический (КДР) и конечно-систолический (КСР) размер, степень укорочения переднезаднего размера (DS), толщину межжелудочковой перегородки (ТМЖП) и задней стенки (ТЗС) ЛЖ, расстояние от точки Е передней створки митрального клапана до межжелудочковой перегородки (МЖП) (E-point septal separation – EPSS), суммарную толщину стенки
(2H – ТМЖП + ТЗС), а также индекс 2H/D (где D – КДР ЛЖ). Диастолическая функция ЛЖ изучена с помощью импульсной допплерэхокардиографии. По данным исследования трансмитрального кровотока оценивали максимальную скорость раннего (Е) и позднего (А) диастолического наполнения ЛЖ, их соотношение (Е/А), время изоволюмической релаксации (ВИР) и замедления раннего диастолического наполнения (ВЗЕ).
При определении эхокардиографических критериев ИКМП мы ориентировались на эхо-индекс Керена, предложенный для оценки выраженности позднего ремоделирования ЛЖ у больных, перенесших острый
Q-ИМ [7]. Дополнив его еще одним параметром – ФВ менее 50%, мы установили следующие ориентировочные эхокардиографические критерии ИКМП: КДР ЛЖ более 57 мм, ФВ менее 50%, DS менее 24%, митрально-септальная сепарация (МСС) более 10 мм. У пациентов с ИБС при наличии не менее трех компонентов эхо-индекса (более 3) формирование ИКМП считали высоковероятным. Учитывая особенности нарушения внутрисердечной гемодинамики и тактики лечения, больных с хронической аневризмой ЛЖ в данное исследование не включили, результаты их эхокардиографии опубликованы нами ранее [2].Для оценки диагностической значимости предложенных эхокардиографических критериев ИКМП мы сравнивали их с показателями у 227 больных, перенесших ИМ более одного года назад, у которых эхо-индекс не превышал 2. При постинфарктном кардиосклерозе (ПИК) дисфункция сосочковых мышц способствует возникновению митральной регургитации, что часто обусловливает дилатациюЛЖ и левого предсердия (ЛП) [3]. При этом у некоторых больных КДР ЛЖ превышает 60 мм. Обычно при сохранении сократительной способности ЛЖ компенсаторно увеличивается амплитуда движения его стенки, что поддерживает DS и ФВ в нормальных пределах, может уменьшаться расстояние EPSS. Без других компонентов эхо-индекса увеличение КДРЛЖ не считали диагностическим критерием КМП. Кроме больных с ПИК, в группу сравнения включены 40 здоровых лиц, сопоставимых по полу и возрасту.
В зависимости от выраженности систолической дисфункции ЛЖ больные с ИКМП распределены на 3 группы: I группа – с умеренно выраженным снижением сократимости (ФВ в пределах 40–50%); II группа – с систолической дисфункцией средней тяжести (ФВ от 30 до 40%); III группа – с выраженным снижением ФВ (менее 30%).
Результаты и их обсуждение
У больных с ИКМП и ПИК переднезадний размер ЛП, КДР, КСР, КДО и КСО ЛЖ достоверно превышали соответствующие показатели у здоровых лиц, величины DS и ФВ были ниже (табл. 1). Максимальные величины КДР, КСР, КДО и КСО и минимальные DS и ФВ отмечены у больных III группы, они достоверно (P<0,05) отличались от таковых у больных I группы. При сравнении соответствующих показателей у больных с ИКМП и ПИК с ФВ 40–50% выявлено увеличение КДР, КСР, КДО и КСО, а также уменьшение DS и ФВ, однако различия их были недостоверны.
Эти показатели достоверно отличались от таковых у больных с ПИК, у которых ФВ превышала 50%. Уменьшение DS сопровождалось увеличением EPSS, наибольшим оно было у больных III группы с ИКМП.Таблица 1 Основные показатели внутрисердечной гемодинамики у больных с ИКМП 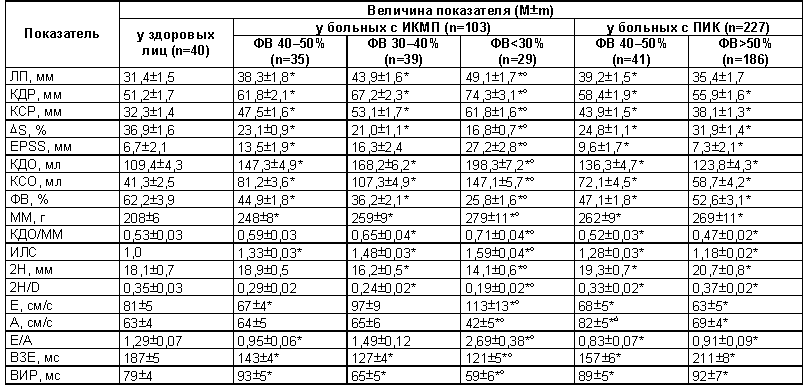
Примечание. Различия показателей достоверны по сравнению с таковыми: * – у здоровых лиц; D – у больных с ПИК с ФВ 40–50%; ° – у больных I и III групп с ИКМП (P<0,05).
ММ ЛЖ, индекс КДО/ММ у всех больных достоверно отличались от таковых у здоровых лиц. При сравнении средней величины ММ у больных с ИКМП и ПИК с ФВ 40–50% и с ФВ более 50% достоверные различия не выявлены. Однако при сравнении индекса КДО/ММ отмечено, что степень увеличения КДО более выражена, чем прирост ММ у больных I группы с ИКМП. Наибольшая величина этого индекса установлена у больных III группы (ФВ менее 30%). Увеличение этого индекса обусловлено повышенной нагрузкой на стенку ЛЖ (нагрузка на стенку ЛЖ прямо пропорциональна его внутреннему размеру и давлению и обратно пропорциональна толщине его стенки), это свидетельствовало, что гипертрофия ЛЖ не может компенсировать увеличение его объема [13]. У этих больных наблюдали наименьшее значение 2Н и 2H/D, что обусловлено истончением миокарда. У них же намного чаще выявляли зоны акинезии-дискинезии с наличием демаркационной линии.
Величина ИЛС напрямую зависела от количества сегментов с асинергией, особенно от наличия акинезии и дискинезии. При ИКМП акинезия-дискинезия двух сегментов и более со значительным уменьшением толщины миокарда отмечена у 43 (41,7%) больных, явная демаркационная линия – у 21 (20,4%), гипокинезия более 3 сегментов с различной локализацией – у 53. Акинезию-дискинезию по передне-перегородочной области регистрировали чаще – у 29 (28,2%) больных.
Выявлена обратная зависимость между ИЛС и ФВ. Наибольший ИЛС наблюдали у больных III группы, ему соответствовала наименьшая ФВ.
При сравнении ИЛС у больных с ИКМП и ПИК с ФВ 40–50% достоверные различия не обнаружены, однако он достоверно отличался от соответствующего показателя у больных с ПИК, у которых ФВ превышала 50%.
При изучении параметров диастолической функции ЛЖ установлено, что у пациентов с ИБС как с ФВ, превышающей 50%, так и находящейся в пределах 40–50%, отмечено достоверное (P<0,05) снижение отношения Е/А по сравнению с таковым у здоровых лиц, но внутригрупповые различиябыли недостоверными. У больных с ИКМП при хронической СН III и IV ФК наблюдали значительное увеличение скорости наполнения в ранней (Е) и снижение в поздней (А) диастоле, тем самым расслабление миокарда становилось вначале (у больных с СН III ФК) псевдонормальным, а затем (IV ФК) – рестриктивным. Рестриктивный тип расслабления ЛЖ у больных с ИКМП при хронической СН IV ФК проявлялся также достоверным уменьшением ВИР и замедлением раннего диастолического наполнения.
Нами изучена частота возникновения систолической и диастолической дисфункции ЛЖ в зависимости от ФК хронической СН у больных с ИКМП и ПИК (табл. 2). При этом мы учитывали три величины ФВ – 45–50, 40–45 и менее 40%. Систолическая дисфункция ЛЖ у больных с ИКМП и ПИК с хронической СН II ФК при ФВ 45–50% обнаружена соответственно у 11 (10,7%) и 18 (7,9%) больных, различия статистически недостоверны; при ФВ 40–45% – у 25 (24,4%) и 9 (4%), различия статистически достоверны.
У всех больных с ИКМП при хронической СН IV ФК ФВ не превышала 40%.Таблица 2 Сравнительная характеристика больных с хронической сердечной недостаточностью с учетом систолической и диастолической дисфункции ЛЖ
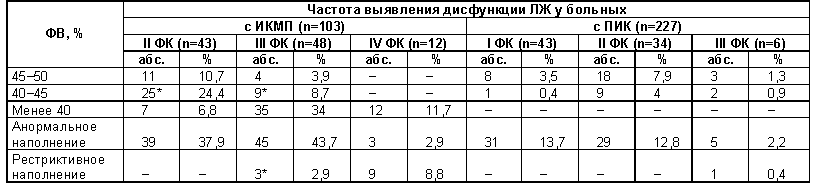
Примечание. Различия частоты систолической и диастолической дисфункции у больных с ИКМП и ПИК с соответствующим ФК хронической СН достоверны (P<0,05).
Хроническая СН III ФК отмечена у 6 (2,6%) больных с ПИК, у 5 из них ФВ была в пределах 40–50%. Анормальное расслабление ЛЖ выявлено у 5 (2,2%) больных, рестриктивное – у 1 (0,4%). У больного с рестриктивным наполнением КДР ЛЖсоставлял 54 мм, ФВ – 43%. Из больных с анормальным расслаблением у одного КДР ЛЖ составлял 59 мм, ФВ – 51%, еще у одного – соответственно 56 мм и 46%. ИЛС у больного с рестриктивным наполнением составлял 1,31, с анормальным расслаблением и ФВ 46% – 1,38. С учетом клинических данных двое из этих больных для дальнейшего наблюдения переведены в группу с ИКМП.
Проведено динамическое наблюдение за 19 больными с ИКМП с момента начала острого Q-ИМ (12 – передней локализации, 7 – задней). К концу госпитального периода КДР ЛЖ составлял в среднем (59,8±3,7) мм, DS – (24,7±0,8)%, ФВ – (48,1±1,8)%, ИЛС – 1,41±0,03. У 11 больных выявлена акинезия-дискинезия более 2 сегментов. Через 1 год после начала острого ИМ отмечали все признаки ИКМП, эхокардиографические показатели составляли: КДР ЛЖ – (67,9±4,1) мм, DS – (22,4±0,8)%, ФВ – (42,8±1,9)%, ИЛС – 1,45±0,03.
Выводы
- Характерными эхокардиографическими показателями ИКМП у пациентов с ИБС являются: КДР ЛЖ – более 57 мм, ФВ – менее 45%, DS – менее 24%, EPSS – более 10 мм, 2H/D – менее 0,30, ИЛС – более 1,31, наличие диастолической дисфункции ЛЖ.
- Для тяжелой формы ИКМП характерно сочетание следующих эхокардиографических показателей: КДР – более 70 мм, ФВ – менее 30%, DS – менее 20%, EPSS – более 20 мм, 2H/D – менее 0,20, ИЛС – более 1,5, рестриктивное наполнение ЛЖ: Е/А в среднем 2,69±0,38, ВЗЕ – (121±5) мс, ВИР – (59±6) мс.
- При хронической СН III ФК у пациентов с ИБС, даже если линейные параметры ЛЖ остаются в пределах нормы, наличие диастолической дисфункции, ФВ менее 50% и высокий ИЛС (более 1,31) позволяют установить диагноз ИКМП.
- Наличие акинезии-дискинезии пораженных сегментов, КДР более (59,8±3,7) мм, ФВ – менее 50%, ИЛС – более 1,38 к концу госпитального периода у больных с острым ИМ свидетельствуют о формировании у них ИКМП.
- Абдуллаєв Р.Я. Ехокардіографічна діагностика ішемічної кардіоміопатії // Укр. радіол. журн. – 2001. – № 1. – С. 50-54.
- Абдуллаєв Р.Я. Ехокардіографічна діагностика дисфункції лівого шлуночка у хворих із хронічною постінфарктною аневризмою // Укр. радіол. журн. – 2001. – № 2. – С. 219-222.
- Абдуллаєв Р.Я. Ехокардіографічна діагностика мітральної недостаності у хворих на постінфарктний кардіосклероз // Укр. радіол. журн. – 2001. – № 3. – С. 270-272.
- Никитин Н.П., Аляви А.Л., Голоскокова В.Ю., Маджитов Х.Х. Особенности процесса позднего ремоделирования сердца у больных, перенесших инфаркт миокарда, и их прогностическое значение // Кардиология. – 1999. – № 1. – С. 54-58.
- Chon J.N. Critical review of heart failure: the role of left ventricular remodelling in the therapeuticrespons // Clin. Cardiology. – 1995. – Vol. 18 (Suppl. IV). – P. 4-12.
- Hare J.M., Walford G.D., Hruban R.H. et al. Ischemic cardiomyopathy: endomyocardial biopsy and ventriculographic evaluation of patients with congestive heart failure, dilated cardiomyopathy and coronary artery disease // J. Amer. Coll. Cardiology. – 1992. – Vol. 20. – P. 1318-1325.
- Keren A., Gottlieb S., Arbov Y. et al. Usefulness of predischarge echocardiographic criteria in predicting complications following acute myocardial infarction // Cardiology. – 1986. – Vol. 73. – P. 139-146.
- Macor F., Antonini-Canterin F., Ascione L. et al. Left atrial remodelling after acute myocardial infarction: an analysis of the GISSI-3 echo substudy // Europ. Heart J. – 1999. – Vol. 20 (Abstr. suppl). – P. 527.
- Mitchell G.F., Lamas G.A., Vaughan D.E. et al. Left ventricular remodelling in the year following first anterior myocardial infarction: A quantitative analysis of contractile segment lengths and ventricular shape // J. Amer. Coll. Cardiology. – 1992. – Vol. 19. – P. 1136.
- Pfeffer M.R., Crossman W., Lorell B.H. Hemodynamic aspects of left ventricular remodelling after myocardial infarction // Circulation. – 1993. – Vol. 87, № 7. – P. 28-30.
- Recommendations for quantification of the left ventricle by two-dimensional echocardiography (Amer. Soc. of Echocard. Committee on Standards) // J. Amer. Soc. Echo. – 1989. – № 2. – P. 358-367.
- Sawada S.G., Ryan T., Segar D. et al. Distinguishing ischemic cardiomyopathy from nonischemic dilated cardiomyopathy with coronary echocardiography // Amer. Heart J. – 1992. – Vol. 19. – P. 1223.
- Schiller N.B. Two-dimensional echocardiographic determination of left ventricular volume, systolic function, andmass. Summary and discussion of the 1989 recommendations of the American Society of Echocardiography // Circulation. – 1991. – Vol. 84 (Suppl. 3). – P. 280.
- Sharp S.M., Sawada S.G., Segar D.S. et al. Dobutamine stress echocardiography: detection of coronary artery disease in patients with dilated cardiomyopathy // J. Amer. Coll. Cardiology. – 1994. – Vol. 24. – P. 934-939.
- Spinale F.G. Novel Approaches to retard ventricular remodelling in heart failure // Europ. J. Heart Failure. – 1999. – Vol. 1. – P. 17-23.
Echocardiographic parameters of left ventricular systolic and diastolic function in ischemic cardiomyopathy
R.Ya. Abdullayev
The aim of the study was to determine the peculiarities of left ventricular systolic and diastolic function in patients with ischemic cardiomyopathy. 103 pts have been included into the study. Akinesis and dyskinesis with myocardium wall thinning has been observed in 43 patients, evident border line – in 21 patients. Hypokinesis of more than three segments of different localization was registered in 57 patients. Decreased ejection fraction (EF) was observed in all patients, i.e. EF 40–50% in 49 pts, EF 30–40% – in 41 pts and EF<30% – in 13 pts respectively. Highest local contractility index (LCI), end-diastolic and systolic diameter (EDD, ESD) of the left ventricle was registered in pts with EF<30%. The restrictive diastolic dysfunction was observed in 12 pts – 3 from them with EF of 30–40% and 9 with EF<30%.

Ваш комментарий