Терапия-Раздел 7. Вспомогательные средства лечения ХСН
Раздел 7. Вспомогательные средства лечения ХСН
Член-корр. РАН, проф. Ю.Н. Беленков, проф. В. Ю. Мареев
URL
7.1.9. Нитровазодилататоры
в лечении ХСН
Как видно из рис. 73, препараты, получившие название
нитровазодилататоров и применяющиеся в качестве вазодилатирующих
препаратов в комплексном лечении ХСН, оказывают свое действие
через стимуляцию образования цГМФ. Образование цГМФ в ГМК способствует
их расслаблению и снижению тонуса периферических сосудов. Поскольку
нитраты преимущественно венозные вазодилататоры, скорее можно
говорить об их способности увеличивать растяжимость вен.
Механизм действия нитровазодилататоров представлен на рис.
75. Как видно, существует три разновидности
нитровазодилататоров, имеющих особенности действия на образование
цГМФ.
Органические нитраты (нитроглицерин, ИСДН) после метаболизации в печени до 2- и 5 - ИСМН (понятно,
что ИСМН не метаболизирует в печени и обладает
максимальной биодоступностью) попадают в ГМК. Далее происходит
цепочка превращений с участием глютатион редуктазы до NO. После
чего, соединяясь со свободными SH-группами, они превращаются в
нитрозотиол (R-SNO), который стимулирует гуанилатциклазу
и активирует образование цГМФ, определяющего расслабление
ГМК. Как понятно, на длинном пути превращения от нитритов (R-NO2)
до нитрозотиолов недостаточная активность ферментных систем или
свободных SH-групп может приводить к потере эффективности нитратов,
при их сохранной концентрации в крови. Такое состояние
получило название толерантности к нитратам. Хотя в последние годы
многие авторы сомневаются в обязательности образования нитрозотиолов
для вазодилатирующей эффективности нитратов.
Другой нитровазодилататор, молзидомин, метаболизируя
в печени до своего активного метаболита SIN -1, стимулирует выработку
эндотелием специфического ЭДРФ. ЭДРФ (идентичный NO) напрямую
стимулирует гуанилатциклазу ГМК, приводя к их расслаблению и вазодилатации.
Путь от лекарства к стимуляции гуанилатциклазы короче и не связан
с внутриклеточными превращениями. На этом основании было предположено,
что молзидомин не должен вызывать толерантности. Однако специальные
исследования доказали, что это не так. Молзидомин также вызывает
“привыкание” и со временем теряет свою вазодилатирующую активность.
Отсюда можно сделать вывод, что теория толерантности к нитратам,
связанная с исчерпанием свободных SH-групп, выглядит весьма сомнительной.
Поэтому сегодня господствует точка зрения, что толерантность к нитровазодилататорам может быть связана
с рефлекторным повышением гормонов (САС, РААС и др.). Одним из
способов предотвращения толерантности к нитратам является применение
ИАПФ. Если бы теория толерантности, связанная с истощением сульфгидрильных
групп, была верна, то ИАПФ каптоприл, имеющий в своей молекуле
SH-группу, превосходил другие ИАПФ по способности прерывать толерантность
к нитратам. Практика же показала идентичность разных по химической
структуре ИАПФ в прерывании толерантности к нитропрепаратам. К
другим возможным механизмам толерантности к нитратам относят потерю
чувствительности гуанилатциклазы, увеличение объема внутрисосудистой
жидкости и оксидативный стресс, преобразующий нитраты в пероксинитриты,
которые резко повышают чувствительность ГМК к вазоконстрикторным
агентам.
Так или иначе, но нитраты и молзидомин, как подробно обсуждалось
в разделе 7.1.4, снижают уровень венозного возврата и перегрузку
малого круга кровообращения, практически не влияя на артериолярный
тонус и не изменяя величины СВ. В табл. 16 на стр. 218 были представлены
гемодинамические эффекты ИСДН и молзидомина.
ИСДН (нитросорбид), применявшийся в дозах от 120 мг (40 мг 3 раза) до 240 мг
(60 мг 4 раза), в среднем 136 мг/сут, выглядел как типичный венозный
вазодилататор. Венозный тонус достоверно снижался на 30%, при
этом уменьшалась перегрузка малого круга кровообращения и ДЗЛА
на 33%. Больные субъективно чувствовали уменьшение одышки, хотя
около 40% пациентов при применении таких высоких доз ощущало головные
боли. Артериолярный тонус снижался мало и СВ не изменялся (см.
табл. 17 на стр. 222).
В настоящее время ИСДН доступен
в виде кардикета, изокета, изомака -ретарда и др.
В последние годы в клинике, как
мы уже упоминали, применяется новый нитровазодилататор ИСМН
(моно мак, мночинкве, эфокс, изомонит гексал ретард и др.).
Этот препарат не метаболизирует в печени, быстро достигает
высокой концентрации в плазме и имеет большую продолжительность
действия. Это позволяет применять ИСМН в дозах 20 - 40
мг дважды, а ретардные формы даже
1 раз в сутки.
Молзидомин (корватон)
исследовался в двух дозах – 12 мг/сут
(4 мг 3 раза) и 24 мг/сут (8 мг/сут 3 раза). В малых дозах он
действовал как венозный вазодилататор (снижение венозного тонуса
на 22% и ДЗЛА на 20%). При двукратном увеличении дозы препарата проявилось его
артериолодилатирующее действие (снижение артериолярного тонуса
на 14% и адекватное увеличение СИ на 12%). При этом венодилатирующее
действие не менялось. Это типично для нитровазодилататоров:
при низких дозах они увеличивают растяжимость вен и не влияют
на тонус артериол, при увеличении дозы их венодилатирующее действие
не усиливается, но они начинают снижать артериолярную вазоконстрикцию.
Поэтому при применении нитровазодилататоров важно решить,
с какой целью вы их будете применять
– для симптоматического улучшения у больных с перегрузкой малого
круга (обычно используется в острых ситуациях) или как системный
вазодилататор (практически не используется), или просто как симптоматическое
средство для купирования стенокардии у больных с ХСН ишемической
этиологии.
Важно помнить, что, несмотря на
более чем столетнюю историю, нитраты ни при одной патологии, тем более при ХСН, не
показали способности улучшать прогноз больных. Ретроспективный анализ применения вазодилататоров у больных
с клинически выраженной ХСН (II - IV ФК), проводившийся в отделе
сердечной недостаточности НИИ кардиологии им. А.Л.Мясникова РКНПК
Минздрава РФ, выполненный на материале 464 больных, показал достоверное
увеличение риска смерти у больных с клапанными пороками сердца
на 33% (р<0,001), а у больных с ДКМП на 17% (недостоверно).
В группе пациентов с ишемической этиологией ХСН, у которых как
раз логично и требуется назначение нитропрепаратов, риск смерти,
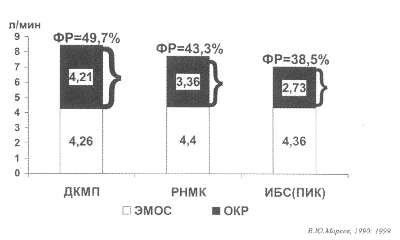
хотя и недостоверно, увеличивался на 15% (рис. 76). Причем видно,
что смертность через 2 года лечения в группе лечения нитратами
составляла 64% против 45% в группе контроля (p = 0,07).
Поэтому в любом случае их применение
будет симптоматическим, а следовательно, вряд ли есть необходимость
стремиться к назначению очень высоких дозировок этих препаратов
больным с ХСН. Кроме того, у 80% больных через несколько недель
лечения разовьется толерантность к действию нитровазодилататоров,
и их применение станет бесполезным.
Более того, в 90-е годы, в “эру
ИАПФ”, включение вазодилататоров в комплекс терапии ХСН становится
совсем сомнительным, так как приводит к дополнительному снижению
АД и вынужденному уменьшению дозировок ИАПФ. Анализ крупных исследований
по применению ИАПФ: (SAVE с каптоприлом, SOLVD c эналаприлом, TRACE с трандолаприлом,
GISSI 3 с лизиноприлом) показал, что добавление нитратов к ИАПФ
не меняет прогноз. В исследовании SMILE с зофеноприлом прогноз
при присоединении нитратов достоверно ухудшался (рост смерти с
8,3 до 15,7%, р=0,02). Другими
словами, ни от нитратов как таковых, ни от их комбинации с ИАПФ
не следует ждать улучшения течения и прогноза декомпенсации.
При лечении острой левожелудочковой
недостаточности применение внутривенных форм нитратов
(чаще всего нитроглицерина) по сей день является одним из
основных видов борьбы с сердечной астмой и отеком легких. Нитроглицерин
(перлинганит, нитро, нитро мак и др.) обычно
выпускается в ампулах, на которых указано количество миллиграммов
препарата. После разведения в физиологическом растворе (200,0 - 400,0) вводится внутривенно
капельно медленно, начиная со скорости 0,8 - 1,2 мкг/кг/мин с
последующим повышением темпа инфузии на 1 мкг/ кг/ мин до достижения
оптимальной скорости. Критериями оптимальной скорости введения
препарата считается снижение ЦВД
на 50% от исходного или до величины 5 мм рт.ст. или снижение ДЗЛА
на 50% от исходного или до величины 12 мм рт.ст. При этом системное
АД не должно снижаться ниже 85/60 мм рт.ст. Врачи отделений неотложной
кардиологии очень часто прибегают к одновременной инфузии нитроглицерина
и положительных инотропных агентов (допамина, добутамина). Это
полностью оправдано, так как нитроглицерин слабо влияет на артериолярный
тонус и не увеличивает СВ. Следует лишь помнить, что при высоких
темпах введения указанных инотропных препаратов будет проявляться
их a-стимулирующее действие, которое нивелирует вазодилатирующие
эффекты комбинации препаратов. Эффект нитроглицерина проявляется
уже в первые минуты и продолжается в течение всей инфузии. В экстренной
ситуации, до налаживания должного гемодинамического контроля и
подготовки к инфузии препарата, можно использовать сублингвальную
форму препарата, назначаемую больному под язык каждые 15 мин (конечно,
при контроле АД).
Последним препаратом из группы
нитровазодилататоров является мощнейший вазодилататор, неорганический
нитрит нитропруссид натрия. Этот
препарат (см. рис. 75 на стр. 227) прямо стимулирует выработку
NO в ГМК как артериол, так и венул, вызывая системную вазодилатацию.
В отличие от нитроглицерина
нитропруссид натрия не только разгружает малый круг кровообращения,
но и увеличивает СВ. Однако контроль за его действием должен быть
тщательным, так как за счет артериолодилатации препарат может
сильно снижать АД. Принципы введения и методы контроля такие же,
как для нитроглицерина. В последние годы нитропруссид натрия применяется
реже в связи с токсичностью и способностью метаболизировать с
образованием цианидов и тиоционатов.
| ! | ПВД (нитраты) не влияют на прогноз больных с ХСН или даже ухудшают его (у больных с пороками сердца). Кроме того, дополнительное (к ИАПФ) назначение нитратов может усугублять снижение АД. Это не позволяет достигать оптимальных доз ИАПФ. Поэтому нитраты в комплексном лечении ХСН должны применяться так редко, как это возможно. Показанием к применению нитратов является лишь выраженная стенокардия, при которой доказано положительное действие нитровазодилататоров. |
Большим подспорьем в лечении
острой левожелудочковой недостаточности является внутривенное
введение лазикса. Нет ничего удивительного в том, что мы обратились
к этому вопросу в главе, посвященной венозным вазодилататорам.
Исследования, проводившиеся нашей группой 20 лет назад, убедительно
доказали наличие выраженного венодилатирующего действия у внутривенной
формы лазикса (рис.77). Как видно, немедленный клинический эффект внутривенного
введения лазикса (некоторые пациенты ощущают его буквально “на
игле”) связан не с диуретическим действием, которое развивается
через несколько десятков минут, а с существенным увеличением растяжимости
венул, наблюдающимся уже в первые 3 - 5 мин. Как видно, венодилатирующая
фаза действия лазикса продолжается 40 - 50 мин и в первые 15 мин
после инъекции наблюдается максимальная скорость падения ЦВД,
отражающая величину венозного возврата крови к сердцу. Затем,
после появления диуретического эффекта, начинающегося, как правило,
через 30 мин, наблюдается второй пик снижения ЦВД, как отражение
продолжающейся разгрузки сердца. О двухфазности действия лазикса
должны помнить все врачи, работающие в ургентной медицине. Улучшение клинического
состояния больного с сердечной астмой после внутривенного введения
лазикса не гарантирует стабильности эффекта. Если диуретическое
действие не наступит, после окончания венодилатирующей фазы действия
лазикса отек легких может повториться. Мы неоднократно наблюдали
таких больных. Поэтому “золотым правилом”, особенно для врачей
скорой медицинской помощи, является необходимость дождаться диуретического
действия лазикса. Только после этого можно быть уверенным в достаточности
предпринятых мер.
7.2.3. Амиодарон в лечении
ХСН
Наиболее изученным является производное
бензофурана амиодарон, единственный (за исключением БАБ) антиаритмик,
который подробно исследовался в длительных контролируемых исследованиях
у больных, пренесших ОИМ и имеющих симптомы ХСН. В целом доступны
для анализа данные 13 исследований, включивших более 6500 пациентов,
при длительности наблюдения от 1 года до 5 лет. Из 13 протоколов
в 8 амиодарон исследован у больных после ОИМ, многие из которых
находились в состоянии декомпенсации (5100 больных), и в 5 препарат
назначали для лечения желудочковых нарушений ритма сердца при
ХСН (1452 больных). Несмотря на разнонаправленные результаты отдельных
исследований, метаанализ позволяет выявить положительное действие
амиодарона на выживаемость больных с ХСН. Снижение риска смерти
по всей группе составило 13% (р=0,03), а внезапной смерти – 29%
(р=0,0003). Среди больных с ХСН снижение общей смертности составило
17% и было достоверным, а уменьшение риска внезапной смерти составило
23% и чуть не достигло достоверности (р=0,06).
По результатам исследований GESICA и CHF-STAT определено, что
наибольший эффект амиодарон оказывает у больных с неишемической
этиологией ХСН. Однако и для других пациентов с ХСН при появлении
опасных для жизни желудочковых аритмий в качестве средства выбора
нужно предпочесть амиодарон, максимально эффективный и относительно
безопасный. Особенно вероятен эффект амиодарона у больных с исходно
имеющимися пробежками желудочковой тахикардии.
Главным ограничением к применению амиодарона является большое
количество побочных эффектов, встречающихся при его длительном
применении. Все побочные эффекты терапии амиодароном можно разделить
на опасные для жизни или кардиальные, связанные с проаритмическим
действием, и экстракардиальные.
Учитывая, что основой действия амиодарона как антиаритмика
III класса является селективное удлинение реполяризации и потенциала
действия, проявлением его эффекта является удлинение интервала
QT. Однако это может сопровождаться появлением собственных желудочковых
аритмий с меняющейся проводимостью, получивших название torsades
de pointes (в русскоязычной литературе
– тахикардия типа пируэта как неверный перевод с французского).
Эти злокачественные аритмии являются главным осложнением терапии
антиаритмиками III класса. Более того, имеются сведения, что некоторые
антиаритмики III класса могут провоцировать подобные проаритмии
у больных с ХСН с гораздо большей вероятностью, чем у недекомпенсированных
пациентов. Амиодарон имеет наименьший риск развития таких желудочковых
аритмий – 1,6% против 3,4 % у соталола и около 9% у “чистых” антиаритмиков
III класса (ибутилид, дофетилид, азимилид).
Амиодарон отличается прежде всего тем, что он, строго говоря,
имеет свойства антиаритмиков всех четырех классов: кроме удлинения
реполяризации, он блокирует натриевые токи (аналогично антиаритмикам
I класса), является частичным БАБ, симпатолитиком и блокатором
медленных КК. Кроме того, амиодарон нарушает превращение тироксина
в трийодтиронин. С одной стороны, это частично дополняет антиаритмические
свойства препарата, но с другой – чревато нарушениями функции
щитовидной железы. Скорее всего, благодаря своему уникальному
механизму действия амиодарон и отличается от других препаратов
III класса меньшим числом кардиальных побочных эффектов при сохраняющейся
в условиях декомпенсации антиаритмической активности.
Следует помнить, что амиодарон медленно накапливается в
организме и постепенно выводится (в сроки до нескольких недель
после прекращения лечения). Поэтому это не средство скорой помощи,
хотя в экстренных ситуациях можно воспользоваться внутривенным
введением препарата. Для более быстрого достижения оптимальной
концентрации ранее существовали специальные схемы насыщения амиодароном.
При сердечной недостаточности использование насыщающих доз должно
быть очень осторожным. Максимально допустимый режим – 600 мг в
течение 5 - 7 дней с последующим переводом сразу на поддерживающую
дозу 200 мг/сут. При таких невысоких поддерживающих дозировках
никаких перерывов в лечении амиодароном не требуется. Необходимо
лишь не забывать, что при появлении
побочных реакций и отмене амиодарона больной должен минимум 7-10
дней находиться под наблюдением, пока не произойдет достаточного
уменьшения его концентрации в плазме крови.
К сожалению, часто ограничением к лечению амиодароном, особенно
при ХСН, является развитие многочисленных и разнообразных экстракардиальных
побочных эффектов. Считается, что 75% больных, принимающих
амиодарон в течение 5 лет, страдают от каких-либо осложнений,
связанных с приемом препарата. Наиболее типичные побочные реакции:
гипотиреодизм (7,0%; в 5,9 раза чаще, чем на плацебо), гипертирео-идизм
(1,4%; в 2,5 раза чаще, чем на плацебо), нейропатии (0,5%; в 2,8
раза чаще, чем на плацебо), легочные инфильтраты (1,6%; в 3,1
раза чаще, чем на плацебо), брадикардия (2,4%; в 2,6 раза чаще, чем на плацебо) и нарушения
функции печени (1,0%; в 2,7 раза чаще, чем на плацебо). К этому
можно добавить из наиболее обычных реакций кератопатии и фотодерматоз.
Считается, что инфильтративные изменения в легких, частота встречаемости
которых по результатам некоторых исследований превышает 5%, –
наиболее серьезное осложнение лечения амиодароном, требующее немедленного
прекращения приема препарата. Время возникновения инфильтративных
изменений в легких варьирует от 6 дней (!) до 60 мес после начала
приема амиодарона. При появлении инфильтратов в легких, после
остановки лечения амиодароном рекомендуется назначение кортикостероидных
гормонов, хотя эффективность такого лечения в контролируемых исследованиях
не подтверждена.
Для минимизации этих
и других побочных реакций амиодарон у больных с ХСН рекомендуется
применять в малых дозах – 200 мг/сут. Кроме того, пациент,
находящийся на длительном лечении амиодароном, должен не реже
3 раз в год наблюдаться у терапевта и окулиста. Однако и при применении
невысоких доз амиодарона, к сожалению, сохраняется риск развития
побочных реакций. Так, в Европейском исследовании по применению
амиодарона у больных после инфаркта миокарда (EMIAT) амиодарон применяли в суточной дозе 200 мг, и при этом
число отмен из-за побочных эффектов составило 38,5% против 21,4%
на плацебо. В аналогичном Канадском исследовании (САMIAT)
суточная доза амиодарона составила 300 мг, но вновь число остановок
лечения из-за побочных реакций оказалось выше в группе лечения
амиодароном (26,2%), чем плацебо (13,2%).
7.2.4. Другие возможности антиаритмического лечения при
ХСН
Особенно интересным представляется возможность сочетания
свойств антиаритмиков II (БАБ) и III (амиодарон) классов в лечении
ХСН, так как подобная комбинация потенциально способна повысить
антиаритмический эффект и усилить антифибрилляторное действие,
при минимизации риска развития проаритмических осложнений. Всегда
считалось, что такое сочетание препаратов необходимо применять
с осторожностью. Однако результаты применения подобной комбинации
в лечении больных с ХСН дает пищу для размышлений. Анализ результатов
исследований CIBIS и CIBIS II показал, что многие больные с ХСН,
получавшие БАБ, одновременно лечились и малыми дозами амиодарона
(200 - 300 мг). Результаты этих исследований продемонстрировали,
что сочетанное применение амиодарона с БАБ в лечении ХСН эффективнее,
чем использование каждого из этих препаратов в отдельности, и
не сопровождается ростом побочных реакций. Это практическое
подтверждение рекомендации по возможному использованию комбинации
амиодарона с БАБ у пациентов с ХСН и опасными для жизни нарушениями
сердечного ритма. Следует лишь помнить, что дозы БАБ должны титроваться
очень медленно, а доза амиодарона не превышать 200, максимум 300
мг/сут. Кроме того, необходим контроль за величиной корригированного
интервала QТ. Его величина 480 мс должна заставить быть на чеку,
а при превышении 525 мс лечение амиодароном необходимо прервать.
При сложности или невозможности применения амиодарона в качестве
антиаритмического средства можно использовать небольшие дозы соталола
(соталекса), объединяющего свойства b-блокатора - блокатора кальциевых КК (антиаритмика III
класса). Препарат по антиаритмическому эффекту лишь незначительно
уступает амиодарону, при этом лучше переносится и вызывает гораздо
меньше побочных реакций. Следует лишь помнить о способности соталола
в 4-5% случаев вызывать проаритмии, в том числе и желудочковую
тахикардию с меняющейся проводимостью. Идеологически применение
соталола близко к использованию комбинации амиодарона с БАБ, поскольку
обеспечивает не только стабильный антиаритмический эффект, но
и антифибрилляторное действие.
| ! | Антиаритмические средства используются лишь при сочетании ХСН с опасными для жизни желудочковыми аритмиями. В качестве средств выбора можно отметить амиодарон (кордарон), применяемый в дозах до 200 мг/сут, и соталол (соталекс), назначаемый в дозах, начиная с 20 мг дважды в сутки, до максимально 160 мг дважды в сутки. Учитывая выраженные b-блокирующие свойства соталола, принцип медленного титрования дозы соответствует описанному для БАБ. |
Рис. 76. Выживаемость больных с ИБС и ХСН III-IV ФК в зависимости от применения НИТРАТОВ
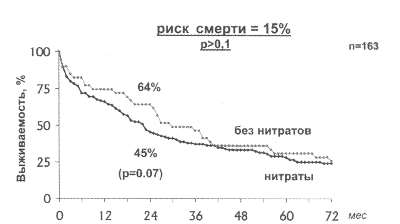
Рис. 77. Динамика растяжимости вен, скорости изменений ЦВД и диуреза после внутривенного введения лазикса больным с ХСН и признаками левожелудочковой недостаточности
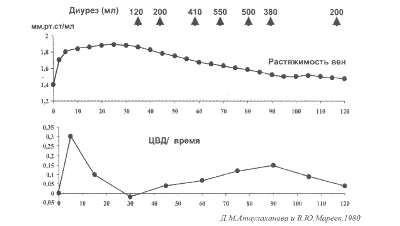
Рис. 78. Соотношения между эффективным минутным объемом сердца (ЭМОС) и объемом клапанной регургитации (ОКР) = фракция регургитации (ФР) при разных заболеваниях, сопровождающихся симптомами ХСН
7.2.5 Немедикаментозное воздействие
на нарушения ритма при ХСН
Следует отметить, что в последние годы большое внимание
уделяется немедикаментозным способам борьбы с опасными для жизни
желудочковыми нарушениями сердечного ритма. Основным способом
такого лечения является имплантация кардиовертера - дефибриллятора
(ИКД). Принцип этого устройства близок к идее кардиостимулятора.
Электроды, располагаемые в эндокарде, позволяют осуществлять контроль
за внутрисердечной электрокардиографией (ЭКГ) и при появлении
длительной желудочковой тахикардии или фибрилляции желудочков
устройство, располагаемое подкожно в области передней поверхности
грудной клетки (чаще всего в подключичной области), производит разряд, позволяющий
купировать приступ опасной для жизни аритмии. Хотя опыт использования
таких устройств пока не очень велик, перспективность такого подхода
для лечения критических больных очевидна.
В настоящий момент имеются результаты трех крупных исследований,
в которых сравнивалась антиаритмическая терапия (в основном амиодарон
и у части пациентов соталол) с ИКД среди пациентов с низкой ФВ.
Первым был протокол MADIT, включивший 196 больных с постинфарктным кардиосклерозом,
ФВ < 35% и непостоянными желудочковыми тахикардиями при суточном
ЭКГ-мониторировании. В итоге в группе медикаментозного лечения
было зафиксировано 39 смертей (27 сердечно-сосудистых), а в группе
ИКД – 15 смертей (11 сердечно-сосудистых). Снижение риска смерти
при применении ИКД составило 54% и было достоверным (p=0,009).
В исследовании AVID обследовали 1016 пациентов с ФВ < 40%, имевших в анамнезе
внезапную смерть или зафиксированную желудочковую тахикардию и
фибрилляцию желудочков. Снижение риска смерти при применении ИКД
в сравнении с антиаритмической терапией составило 39% через 1
год, 27% через 2 года и 31% через 3 года наблюдения. Преимущество
ИКД было достоверным (р< 0,02). В третьем исследовании CABG-PATCH было обследовано 900 больных с ИБС, ФВ < 36%, имевших
изменения на сигнал усредненной ЭКГ. В этом исследовании, продолжавшемся
в среднем 32 мес, рассматривалась возможность профилактического
использования ИКД. В итоге не было выявлено достоверных различий
между антиаритмической терапией и постановкой дефибриллятора. Общее число смертей составило
101 в группе ИКД против 95 в группе медикаментозной терапии и
71 сердечно-сосудистая смерть против 72 в тех же группах соответственно.
Рис. 79. Влияние вазодилататоров на величину
клапанной регургитации при ревматической (РНМК) и относительной
(ОНМК) митральной недостаточности
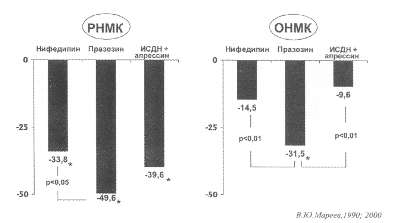
Рис. 80. Влияние вазодилататоров на сердечный индекс (СИ) и объем клапанной регургитации (ОКР) у больных с относительной недостаточностью митрального клапана при ДКМП и ИБС
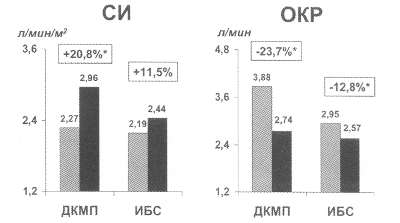
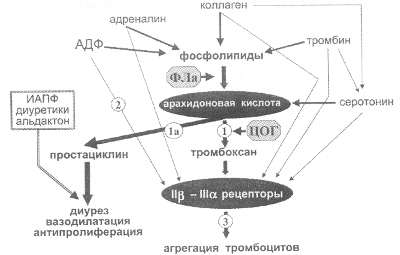
Рис. 81. Механизм действия дезагрегационных препаратов
Для окончательного ответа на
вопрос о целесообразности и эффективности применения ИКД у больных
с ХСН и риском внезапной смерти проводится исследование SCD-HeFT, предполагающее включение 2500 больных с ФВ < 35% и
симптомами ХСН II - III ФК. В настоящий момент уже обследуется
более 1700 пациентов. Однако даже сегодня можно констатировать,
что применение ИКД позволяет снижать риск внезапной смерти декомпенсированных
больных высокого риска (по крайней мере имевших внезапную смерть
или фибрилляцию желудочков в анамнезе). Главной проблемой является
фармакоэкономические показатели, так как стоимость этих устройств
все еще очень высока. Кроме этого, нельзя рассматривать постановку
ИКД как альтернативу антиаритмическому лечению. Дополнительное
использование антиаритмиков позволяет снизить частоту разрядов
ИКД в ответ на развитие опасных для жизни желудочковых аритмий
и продлить эксплуатацию батарей и эффективной работы дефибриллятора.
Лучшим дополнением к ИКД является соталол (соталекс), позволяющий
достоверно уменьшать число
и мощность разрядов ИКД. 7.3. Аспирин и другие дезагреганты
7.3.1. Механизм действия и выбор дозы при ХСН
Аспирин, как хорошо известно, применяется в качестве одного
из основных средств вторичной профилактики у больных, перенесших
инфаркт миокарда. Задачей применения аспирина является нарушение
повышенной агрегации тромбоцитов, которая играет существенную
роль в развитии и прогрессировании коронарного синдрома. Как видно
из рис. 81, конечным фактором, определяющим способность тромбоцитов
к “склеванию” и агрегации, являются специфические рецепторы, получившие
название II бета - III альфа-рецепторов. Все стимулы, способные
усиливать агрегацию тромбоцитов (АДФ, адреналин, серотонин, тромбин,
коллаген, тромбоксан и др.), в конечном счете активируют II бета
- III альфа- рецепторы тромбоцитов. Исходя из этого, смысл использования
антиагрегантов – это прерывание стимуляции специфических рецепторов
тромбоцитов. В клинической практике используются препараты, влияющие
на образование тромбоксана (аспирин), на АДФ-стимулируемую агрегацию (тиклопидин и клопидогрель)
и непосредственные блокаторы II бета - III альфа-рецепторов тромбоцитов.
На рис. 81 точки приложения их действия обозначены цифрами 1,
2 и 3 соответственно. Как следует из рисунка, использование специфических
блокаторов II бета - III альфа-рецепторов тромбоцитов выглядит
наиболее обоснованным, так как позволяет блокировать агрегацию,
стимулируемую любыми агентами, однако, к сожалению, на практике
использование пероральных препаратов этого класса пока успехом
не увенчалось. В подавляющем большинстве случаев основным антиагрегационным
препаратом остается аспирин.
Как видно, основным компонентом биохимического каскада, приводящего
к росту агрегации тромбоцитов, является арахидоновая кислота,
образующаяся из фосфолипидов под действием фосфолипазы А (ФЛа).
Основным механизмом действия аспирина является ингибирование
фермента циклооксигеназы (ЦОГ), в результате чего нарушается синтез
циклических эндоперекисей из арахидоновой кислоты (эта ступень
для простоты изложения на
рис. 81 устранена). В итоге нарушается синтез тромбоксана в тромбоцитах
(показано цифрой 1) и проявляются дезагрегационные свойства препарата.
К сожалению, ингибирование ЦОГ аспирином сопровождается и нарушением
синтеза простациклина и вазодилатирующих простаноидов (показано цифрой 1а). При
ХСН этот эффект сам по себе может оказывать негативное действие
на течение ХСН, приводя к усилению вазоконстрикции и уменьшению
диуреза. Кроме этого, ряд эффектов основных средств лечения ХСН,
прежде всего ИАПФ, реализуется через активацию синтеза простациклинов,
стимулирующуюся брадикинином (см. рис. 24 на стр. 62). Поэтому
с теоретических позиций сочетание аспирина, ИАПФ и диуретиков
не выглядит оптимальным. Аналогичным негативным действием могут
обладать и другие нестероидные противовоспалительные препараты
(НСПВП), имеющие основой действия ингибирование ЦОГ (диклофенак,
индометацин, ибупрофен и др.).
Особенную важность при применении аспирина у больных с
ХСН приобретает выбор оптимальных дозировок. Существуют обоснованные
предположения о том, что для достижения необходимого дезагрегационного
эффекта достаточно очень малых доз аспирина (до 75 мг). Аспирин
необратимо блокирует активность ЦОГ, а тромбоциты как безъядерные
клетки не могут ее ресинтезировать, что обеспечивает длительный
антиагрегационный эффект малых доз препарата. Более того, результаты
клинических исследований подтверждают эти предположения. Аспирин
в дозах от 0,5 до 1,5 г позволяет на 21% снизить риск инфаркта,
инсульта и смерти из-за тромбоэмболий, при дозах от 160 до 325
мг – на 28%, а при дозировках менее 160 мг – на 26%, причем все
различия статистически недостоверны. В то же время при использовании
малых доз аспирина (показано цифрой 1 на рис. 81) его влияние
на системный синтез простациклина значительно ослабевает, что
выгодно для больных с ХСН. Таким образом, пациентам, перенесшим
ОИМ и имеющим признаки ХСН, можно рекомендовать использование
малых доз аспирина (75 - 150 мг). В качестве таких препаратов
целесообразно использовать аспирин кардио (таблетки по 100 мг
и 300 мг) и тромбо АСС (таблетки по 50 и 100 мг), которые
легко дозировать у кардиологических больных.
7.3.2. Эффективность аспирина при ХСН
Специальных исследований по применению аспирина при
ХСН не проводилось, однако значительная база данных из крупных
исследований по ХСН с другими препаратами позволяет сделать некоторые
заключения. Так, в исследовании SAVE c каптоприлом было показано,
что применение аспирина ассоциировалось со снижением риска инсульта
на 56%, причем этот эффект
был более выражен у пациентов с низкой ФВ < 28%. В самом крупном
исследовании SOLVD c эналаприлом (более 6500 больных) более 3000
пациентов одновременно лечились аспирином. Прием аспирина ассоциировался
не только со снижением риска тромбоэмболических осложнений (на
53% у женщин и на 23% у мужчин), но и с достоверным уменьшением
риска смерти (на 18%). При этом достоверно уменьшалась частота
внезапных смертей на 22%, в то время как смертность от прогрессирования
ХСН снижалась недостоверно (на 8%). Представленные данные позволяют говорить о целесообразности
назначения аспирина больным с ХСН и подтверждают необходимость
сохранения его в комплексе лечения пациентов, у которых после
перенесенного инфаркта миокарда развивается декомпенсация сердечной
деятельности. Но нельзя забывать, что при ХСН, требующей назначения
ИАПФ и мочегонных, эффект которых может ослабевать на фоне лечения
аспирином, перед врачом стоит дилемма: что важнее - профилактическое
или лечебное действие аспирина или возможная потеря эффективности
основных средств лечения декомпенсации.
7.3.3. Взаимодействие аспирина и ИАПФ
Как уже не раз упоминалось, 90-е годы в лечении ХСН
являются “эрой ИАПФ”, поэтому каждый препарат, который может претендовать
на место в списке средств лечения декомпенсации, должен быть исследован
на предмет его взаимодействия с ИАПФ. Несмотря на столь значимые
положительные результаты, достигаемые при назначении аспирина,
в последние годы развернулась дискуссия о том, что при сочетанном
применении аспирина и АПФ
эти препараты могут ослаблять и даже полностью нивелировать положительные
свойства друг друга.
7.3.3.1. Теоретические предпосылки негативного взаимодействия
ингибиторов ЦОГ с основными средствами лечения ХСН
Теоретической предпосылкой
к этому явилась способность аспирина блокировать синтез вазодилатирующих
простанидов и простациклина, играющих важную роль в эффектах ИАПФ,
а также активных диуретиков и альдактона. Так, в когортных и ретроспективных
контролируемых исследованиях было продемонстрировано, что аспирин
(в дозах выше 300 мг) и другие НСПВП (индометацин, диклофенак,
ибупрофен и др.) способны более чем в 2 раза увеличивать риск
декомпенсации у больных с ХСН и являются причиной 19% от всех
случаев декомпенсации больных с ХСН. Причем у пожилых больных риск задержки жидкости и обострения декомпенсации
возрастает. Это привело к выводу, что применение аспирина в
высоких дозах, а также индометацина, диклофенака и других НСПВП
в лечении ХСН противопоказано.
Это крайне важная проблема, учитывая частоту использования
НСПВП в реальной жизни. Однако создается впечатление, что эта
проблема в скором времени может быть разрешена. В 90-е годы было
доказано, что в организме имеется две изоформы ЦОГ (ЦОГ-1 и ЦОГ-2).
Первая и основная изоформа поддерживает синтез простагландинов
и простациклина, которые определяют основные физиологические функции
организма (рис. 82). Для ХСН важнейшее значение имеют диурез,
вазодилатация и антипролиферация. Однако в клинике не меньшее
значение придается их способности нормализовывать функцию слизистой
желудка. Вторая изоформа экспрессирует только при стимуляции и
является основным медиатором воспаления. Как видно, в качестве
агонистов выступают провоспалительные цитокины (IL -1, ФНО a) и ростовые факторы. Антагонистами являются противовоспалительные
цитокины (IL-4) и глюкокортикоиды, что, в частности, объясняет
механизм их противовоспалительного действия. Из рис. 82 очевидно,
что изолированное блокирование ЦОГ-2 может позволить достигнуть
желаемого противовоспалительного эффекта и избежать негативных
реакций, прежде всего обострения декомпенсации и поражения желудочно-кишечного
тракта.
Рис. 82. Механизм
действия НСПВП и их взаимодействия с основными средствами лечения
ХСН
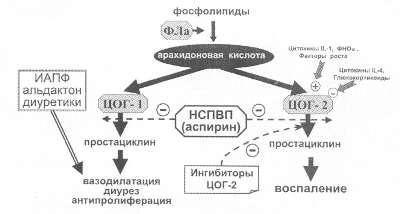
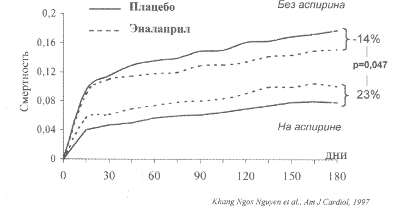
Рис. 83. Влияние ЭНАЛАПРИЛА на общую смертность больных ОИМ в зависимости от сопутствующей терапии АСПИРИНОМ (субанализ CONSENSUS II)
Всем известные НСПВП, такие как
аспирин, диклофенак, индометацин, ибупрофен и др., являются неселективными
ингибиторами обеих изоформ ЦОГ. Поэтому их применение чревато
развитием язв желудка, задержкой жидкости и потерей эффективности
ИАПФ. Выходом из положения может быть использование селективных
антагонистов ЦОГ, недавно появившихся в клинической практике (см.
рис. 82). Первым был препарат мелоксикам, блокирующий ЦОГ -2 в
3 раза сильнее, чем ЦОГ-1. Однако наиболее интересными выглядят
препараты целекоксиб (целебрекс) и рофекоксиб (виокс), позволяющие
блокировать ЦОГ-2 в 375 раз сильнее, чем ЦОГ-1, т.е. представляющие
собой высокоселективные ингибиторы циклооксигеназы - 2. Применение
этих препаратов можно считать средством выбора в лечении воспалительных
процессов у больных с выраженной ХСН.
Для аспирина как неселективного ингибитора ЦОГ выход, как говорилось
выше, видится в использовании малых дозировок, позволяющих блокировать
синтез тромбоксана (цифра 1 на рис. 81), мало нарушая образование
ПГ Е и простациклина. Однако и при использовании малых доз аспирина
эффективность ИАПФ может снижаться. В частности, в только что
опубликованном исследовании было показано, что даже 75 мг
аспирина на 55% снижает вазидилатацию периферических артериол
больных с ХСН в ответ на введение арахидоновой кислоты (A.P.Davies
и соавт.,2000). При дозе 300 мг это снижение составляет 59%. Представленные
сведения свидетельствуют о том, что надежды на большую эффективность
малых доз аспирина в плане блокады тромбоксана, а не простациклина,
могут оказаться необоснованными.
7.3.3.2. Результаты исследований по совместному применению
аспирина и ИАПФ при лечении ХСН
Первой публикацией, подтвердившей негативное взаимодействие
аспирина и ИАПФ, был ретроспективный анализ исследования CONSENSUS
II (рис. 83). На материале более чем 6000 больных очевидна негативная
роль аспирина в действии ИАПФ. В группе пациентов, не получающих
аспирин, смертность при лечении эналаприлом ниже, а среди больных,
дополнительно лечащихся аспирином, положительный эффект ИАПФ пропадает
и смертность даже выше, чем в группе плацебо. Было предемонстрировано,
что сочетание эналаприла с аспирином являлось независимым предиктором
смерти больных с постинфарктным кардиосклерозом (р=0,047).
Похожие результаты были получены при ретроспективном анализе
результатов исследования SOLVD. Положительное влияние аспирина
проявлялось лишь у больных, не получавших эналаприл, и полностью
исчезало в группе лечения ИАПФ. Интересной была оценка и обратного
взаимодействия. Назначение эналаприла сопровождалось достоверным
снижением риска смерти больных с ХСН на 23%, при этом на 29% возрастал
шанс остаться в живых, не иметь обострения ХСН и не быть госпитализированным.
Применение же эналаприла вместе с аспирином приводило хотя и к
недостоверному, но росту риска смерти на 10%, а шанс остаться
в живых и не быть госпитализированным увеличивался только на 19%.
Таким образом, налицо явные негативные последствия сочетания аспирина
и ИАПФ. Аналогичные результаты были получены и в некоторых других
исследованиях.
Однако в 1999 г. были опубликованы и противоположные сведения.
Из базы данных международного исследования по применению беназефибрата,
включающей более 11700 больных,
было выделено 1247 пациентов с ИБС, получавших ИАПФ, а 618 (50%)
из них одновременно лечились аспирином. У 464 из этих пациентов
имелась клинически выраженная ХСН и 221 (47%) из них дополнительно
к ИАПФ получали аспирин. Анализ показал, что при комбинированной
терапии ИАПФ + аспирин риск смерти пациентов с ИБС снижался на
27%, что достоверно больше, чем при изолированном назначении ИАПФ
(19%). Аналогично у больных с ХСН назначение ИАПФ позволяло снизить
риск смерти на 24%, а дополнительное включение в комплекс терапии
аспирина увеличивало шанс на лучший прогноз (снижение риска смерти
на 34%).
Таким образом, однозначного ответа на вопрос, ослабляют
ли малые дозы аспирина эффект ИАПФ у пациентов с ХСН, в настоящее
время нет, и для его решения требуются специальные проспективные
исследования.
Однако уже сегодня очевидно, что больным с ХСН, нуждающимся
в антиагрегационной терапии, гораздо безопаснее назначать не аспирин,
а препараты с другим механизмом действия, не связанным с ЦОГ.
К таким средствам относятся блокаторы АДФ-индуцированной агрегации
тиклопидин (тиклид) и клопидогрель (плавикс).
Тиклид выпускается в виде таблеток по 250 мг и применяется
в суточной дозе 500 мг, назначаемой обычно в 2 приема.
Плавикс выпускается в таблетках по 75 мг и назначается в этой
дозе однократно в сутки. Интересно, что плавикс в дозе 75 мг сравнивался
с аспирином (300 мг/сут) в крупном (более 19 000 больных), многоцентровом,
длительном (1,9 года) рандомизированном исследовании CAPRIE. Результаты этого исследования показали, что клопидогрель
(плавикс) превосходил аспирин и дополнительно на 8,7% снижал риск
инсульта, инфаркта или других сердечно-сосудистых смертей у больных
с ИБС.
Единственным ограничением к применению тиклида или плавикса
может быть более высокая стоимость лечения по сравнению с аспирином.
Но для больных с ХСН замена аспирина на дезагреганты с другим
механизмом действия выглядит наиболее оправданной среди всех других
пациентов.
7.3.4. Аспирин в качестве профилактики тромбоэмболических
осложнений
Еще одна область возможного применения аспирина – профилактика
тромбоэмболических осложнений у больных с мерцательной аритмией.
Как известно, мерцательная аритмия встречается почти у половины
пациентов с ХСН. При этом риск тромбоэмболических осложнений и
инсультов у таких пациентов увеличивается от 2,3 до 6,9 раза.
Метаанализ исследований с аспирином включил более 2500 больных
и продемонстрировал минимальную эффективность этого вида терапии
в качестве профилактики инсультов. Общая смертность при применении
аспирина снизилась с 12,9 до 12,1%, а число инсультов с 11,5 до
9,8%. Эти изменения статистически недостоверны. Однако при этом
и количество кровотечений при применении аспирина не изменилось.
Можно констатировать, что применение аспирина в качестве профилактики
инсультов у больных с ХСН неэффективно и не может быть рекомендовано
к практическому использованию.
В группе больных, перенесших ОИМ, назначение аспирина более
оправдано. Так, в исследовании AMIS аспирин достоверно уменьшал
число инсультов с 0,6 до 0,4%,
хотя и не снижал смертность. При этом риск геморрагий достоверно
возрастал с 0,6 до 1,1%. В другом крупном исследовании PARIS (более
3000 больных после ОИМ) аспирин достоверно уменьшал риск инсультов
с 1,1 до 0,6%. При этом ни смертность, ни частота кровотечений
достоверно не менялись.
Следует отметить, что не все ответы на вопросы о целесообразности
применения аспирина при ХСН могут быть даны сегодня. Требуется
проведение специальных исследований, которые позволят дать более
четкие рекомендации для назначения аспирина в различных клинических
ситуациях больным с декомпенсацией.
| ! | Аспирин применяется в малых дозах (75 - 150 мг/сут) у пациентов с ХСН, в основном на почве постинфарктного кардиосклероза. Особенностью может быть тот факт, что аспирин ослабляет положительное действие ИАПФ. В качестве профилактики тромбоэмболических осложнений применение аспирина эффективно только у пациентов, перенесших инфаркт миокарда. При ХСН из дезагрегантов более оправдано применение тиклида или плавикса. |
7.4. Непрямые антикоагулянты
Вопрос о целесообразности применения непрямых антикоагулянтов
весьма сложен. С одной стороны, при ХСН имеются показания к назначению
оральных антикоагулянтов, а с другой – их применение не безопасно
и предполагает адекватный контроль. К сожалению, в России проблема
с назначением непрямых антикоагулянтов решается очень плохо.
Во-первых, у врачей терапевтов, да и у многих кардиологов
нет традиций и приверженности к использованию препаратов этого
класса.
Во-вторых, в России не
получил распространения самый популярный в мире антикоагулянт
- варфарин. Этот препарат, являющийся производным кумарина, с
80-х годов практически стал синонимом непрямых антикоагулянтов.
В-третьих, в России далеко не во всех лабораториях
измеряется основной показатель эффективности терапии антикоагулянтами,
рекомендованный комитетом экспертов ВОЗ, Международное нормализованное
отношение – (МНО).
Однако при желании все эти трудности преодолимы:
- знания об эффективности оральных коагулянтов и стремление
к лучшим результатам лечения, в том числе и больных с ХСН, могут
изменить отношение врачей к этому виду терапии;
- из кумариновых производных в России имеется синкумар, а в
недалеком будущем появится и варфарин;
- измерение МНО не требует каких-либо
дополнительных затрат в сравнении с измерением более привычного
протромбинового индекса.
Почему же вообще возник вопрос о назначении непрямых антикоагулянтов
больным с ХСН? Ответ прост: само наличие ХСН, при которой развивается
дилатация камер сердца, нередко сопровождается появлением тромбов
в полостях сердца. Это определяет повышенный риск тромбоэмболических
осложнений, в том числе смертельных и приводящих к развитию инсульта.
По результатам исследования SOLVD, включившего более 7000 больных с начальными признаками
декомпенсации (I - II ФК), годичная частота инсультов составила
1,2%. При умеренной и выраженной ХСН II - III ФК (V-HeFT I и II)
частота инсультов составляла 1,8% в год. При тяжелой ХСН III-IV
ФК частота инсультов возрастала до 3,5% (PROMISE) и даже до 4,6%
(CONSENSUS). Иными словами, имеется прямая зависимость между тяжестью
декомпенсации и ростом тромбоэмболических осложнений и инсультов.
Специальных исследований по применению варфарина при ХСН не
проводилось, и имеющиеся данные основаны на ретроспективном анализе
крупных протоколов по лечению ХСН, в которых непрямые антикоагулянты
выступали в роли дополнительного лечения.
В исследовании SOLVD 861 больной находился на терапии варфарином,
что сопровождалось достоверным снижением риска смерти больных
с ХСН на 24%, связанным с приемом антикоагулянта. В двух других
небольших исследованиях применение варфарина ассоциировалось со
снижением риска инсультов соответственно с 3,5 до 0% и с 4 до
1%. Однако в других протоколах варфарин не оказывал влияния на
частоту тромбоэмболий и инсультов, а в исследовании V-HeFT в группе
варфарина число инсультов было даже выше, чем в контроле.
Из представленных данных очевидно, что, несмотря на возможные
перспективы, проблема назначения оральных антикоагулянтов пока
далека от окончательного разрешения.
Гораздо более очевидны показания к применению варфарина у больных,
перенесших ОИМ. По данным исследования WARIS, на материале 1200
больных было показано, что варфарин в сравнении с плацебо (при
достижении величины МНО 2,7-4,8) достоверно снижал не только частоту
инсультов (на 50%), но и риск повторных инфарктов миокарда (на
34%) и общую смертность (на 34%). В другом крупном исследовании
ASPECT, включившем 1400 больных, перенесших ОИМ и получавших лечение
варфарином (МНО=2,8-4,8) в сравнении с плацебо, эти результаты
были подтверждены. Хотя показатель смертности менялся недостоверно,
риск повторного инфаркта миокарда снижался на 53%, а частота инсультов
уменьшалась с 0,8 до 0,4%.
В обоих исследованиях варфарин повышал риск кровотечений (в исследовании
ASPECT c 1,1 до 4,3%), что еще раз подтверждает необходимость
контроля антикоагулянтной терапии.
Большое внимание должно быть уделено и назначению непрямых
антикоагулянтов у больных с ХСН и мерцательной аритмией, когда
риск тромбоэмболий многократно возрастает.
Метаанализ крупных контролируемых исследований, включивших
2900 больных, показал, что варфарин существенно и достоверно уменьшал
частоту инсультов с 8,8 до 3,4% (p<0,0001) и смертность с 12,1
до 6,3% (p<0,01) у больных с мерцательной аритмией. Однако
при этом увеличивался и риск кровотечений с 1,7 до 2,7% (p<0,05).
Представленные результаты позволяют отнести непрямые антикоагулянты
к эффективному способу профилактики тромбоэмболий, инсультов,
внезапной смерти при ХСН и мерцательной аритмии.
Группой риска, для которой применение непрямых антикоагулянтов
становится необходимым, можно считать больных с ХСН старше 65
лет при наличии мерцательной аритмии, тромбоэмболий в анамнезе
и признаках тромбоза ЛЖ, когда опасность тромбоэмболий увеличивается
в 4-7 раз. Но этот вид терапии небезопасен из-за возможности
появления кровотечений (в том числе и интракраниальных гематом).
Эти осложнения наиболее опасны у пожилых больных, у которых применение
антикоагулянтов особенно необходимо. Образно говоря, врач должен
пройти по лезвию – предотвратить развитие тромбоэмболий, не вызывая
побочных реакций. Оптимальным способом контроля за эффективностью
лечения антикоагулянтами является контроль за величиной МНО. Величина
этого показателя 2,0 - 3,0 свидетельствует о хорошей дозе варфарина
(или других антикоагулянтов), а величина МНО выше 3,5 служит сигналом
опасности кровотечений.
7.5. Кортикостероиды
Кортикостероиды используются как вспомогательные средства у
больных с гипотонией (систолическим АД ниже 90 мм рт.ст.), особенно
при необходимости назначения ИАПФ и БАБ. Оптимальной является
доза преднизолона до 30 мг/сут. При обострении декомпенсации преднизолон
может вводиться внутривенно
капельно, особенно перед назначением высоких доз диуретиков. Продолжительность
терапии от 1-2 нед до 2 мес и до достижения оптимальных доз ИАПФ
и/или БАБ. В дальнейшем дозировки преднизолона медленно ступенчато
снижаются по обычной методике. Следует помнить о повышенном риске
желудочно-кишечных кровотечений у больных с ХСН, получающих терапию
кортикостероидами.
Мы касались проблемы назначения кортикостероидов, когда обсуждали
проблему лечения ХСН, протекающей с упорной гипотонией, и при
лечении рефрактерного отечного синдрома. Другого самостоятельного
значения применение этого вида терапии в комплексе лечения декомпенсированных
больных не имеет.
7.6. Статины
Назначение статинов актуально у больных с ИБС и постинфарктным
кардиосклерозом, при наличии у них гиперхолестеринемии. Как известно,
эти препараты являются эффективным средством вторичной профилактики.
Применение статинов у пациентов с ХСН специально не изучалось.
Более того, при проведении исследований со статинами ХСН всегда
считалась противопоказанием к включению больных в протокол. Это
связано с серьезными нарушениями функции печени при ХСН. Как известно,
точкой приложения действия статинов является синтез холестерина
клетками печени. При этом одним из главных побочных эффектов может
быть нарушение функции гепатоцитов и рост трансаминаз. Поэтому
риск назначения холестеринснижающей терапии больным с ХСН, которые
и так нередко имеют повышенный уровень трансаминаз, гораздо выше,
чем в популяции.
С другой стороны, сложен и контроль уровня холестерина. При
серьезной декомпенсации развитие мускатного цирроза печени может
сопровождаться нарушениями синтеза холестерина. В таких случаях
низкий уровень холестерина является предиктором неблагоприятного
течения ХСН.
Единственным свидетельством профилактической роли статинов
в развитии ХСН служат результаты исследования 4S, в котором 4444
больных после перенесенного инфаркта миокарда получали симвастатин
(зокор) или плацебо в течение 5 лет. В начале исследования пациенты
по условиям отбора не имели признаков ХСН, однако за 5 лет наблюдения
признаки декомпенсации развились более чем у 350 пациентов. При
этом симвастатин снижал риск появления ХСН на 23% (p=0,015).
