Офтальмология-Бринзоламид - новый ингибитор карбоангидразы
Бринзоламид - новый ингибитор карбоангидразы
А.А. Хлобыстов, проф. Е.А. Егоров, Т.В. Ставицкая
Российский государственный медицинский университет
URL
Brinzolamide – new carboanhidrase inhibitor
Brinzolamide is the newest inhibitor of human carboanhidrase for topical use. The substance is easy delivered to target tissue, highly selective and has strong inhibiting activity to isoenzyme CA II.
After one–time instillation the maximal effect was registered in 4 hours. The IOP lowered by 18.5% from the base level. In long–term therapy with brinzolamide the IOP level decreased in average by 26.6% in case of two times daily instillation and by 28.8% if the drug was administered three times daily.
The using of brinzolamide is effective as an additional therapy, the combination with timolol gives significant additive effect. Brinzolamide is more well–tolerated than dorzolamide owing to optimal suspension composition and physiological pH.
Brinzolamide doesn’t render systemic effect on human organism.
Первичная открытоугольная глаукома
(ПОУГ) – одна из наиболее частых причин необратимой слепоты. Следует
отметить, что частота слепоты от глаукомы в мире за последние
30 лет практически не изменилась и составляет 14–15% от общего
числа всех слепых [1]. В нашей стране по данным Е.С Либман, отмечается
резкое увеличение роли глаукомы среди причин первичной инвадилизации,
доля которой в нозологической структуре возросла за последние
десятилетие с 12 до 20%, а распространенность с 0,1 до 0,8 на
10 тысяч взрослого населения [4].
А.П. Нестеров в книге «Глаукома» отмечает, что патогенез глаукомы независимо от ее разновидности включает два механизма, разделенных в пространстве и отчасти во времени. Один из них действует в переднем отделе глаза и приводит в конечном итоге к повышению внутриглазного давления (ВГД). Другой механизм, локализующийся в заднем отделе глазного яблока, служит причиной атрофии зрительного нерва. Глаукоматозный процесс начинается в переднем отделе глаза, изменения в зрительном нерве являются следствием действия на него повышенного ВГД.
Ведущим патогенетическим фактором, вызывающим повреждение зрительного нерва и ухудшение зрительных функций, является повышение офтальмотонуса. Повышенное ВГД вызывает механическую деформацию решетчатой пластинки склеры, ущемление в ее канальцах пучков нервных волокон и нарушение микроциркуляции крови в этой зоне. В связи с этим основные методы лечения ПОУГ (медикаментозное, лазерное и хирургическое воздействия) направлены на снижение ВГД до уровня, который предотвращает дальнейшую атрофию волокон зрительного нерва [1,2].
Медикаментозная гипотензивная терапия имеет наибольшее значение в лечении глаукомы. Гамма используемых средств включает разнообразные препараты с различным механизмом гипотензивного действия. В то же время, по данным литературы, у 27–33% больных, страдающих глаукомой и офтальмогипертензией и получающих монотерапию гипотензивными средствами, была выявлена необходимость назначения дополнительных гипотензивных препаратов для нормализации ВГД [2].
Многим больным глаукомой в качестве дополнительной терапии часто назначают пероральные ингибиторы карбоангидразы (ИКА), которые играют важную роль в секреции водянистой влаги. Лекарственный эффект ИКА связан с избирательной способностью угнетать активность карбоангидразы – фермента, участвующего в процессе гидратации и дегидратации угольной кислоты.
Карбоангидраза – фермент, являющийся цинкопротеидом. Содержание цинка 0,33–0,34%. Карбоангидраза впервые была выделена из эритроцитов. В 1 л крови млекопитающих – примерно 1 г карбоангидразы. Наличие этого фермента дает организму возможность освобождаться от избытка СО2. Как правило, КА сосредоточена в клеточных элементах, она не обнаруживается в тканевых жидкостях.
В организме человека данный фермент, который представлен двумя изоферментами КАI и КАII, встречается в эритроцитах, клетках поджелудочной железы, слизистой оболочки желудка, околоушной слюнной железы, почек, ресничного тела глаза.
Карбоангидраза катализирует превращение карбоксида в угольную кислоту (СО2 + H2O = H2CO3). Угольная кислота впоследствии диссоциирует (H+ + HCO3–). Эта реакция – ключ к секреторным физиологическим процессам во многих тканях, в том числе и в глазу.
В результате угнетения активности карбоангидразы в почках происходит уменьшение образования угольной кислоты и снижение реабсорбции бикарбоната и Na+ эпителием канальцев, в связи с чем значительно увеличивается выделение воды. При этом наблюдается повышение pH мочи и потеря ионов калия.
В процессе образования водянистой влаги глаза ионы бикарбоната активно транспортируются в заднюю камеру из цитоплазмы беспигментных клеток, чтобы компенсировать градиент положительных ионов, обусловленный активным транспортом ионов Na+. Ингибиторы КА блокируют образование угольной кислоты, таким образом снижая продукцию HCO3–. В отсутствие достаточного количества ионов HCO3– увеличивается позитивный ионный градиент, что вызывает снижение секреции водянистой влаги. Вероятно, это тот механизм, за счет которого ИКА снижают ВГД.
Первый препарат из группы ингибиторов КА – ацетазоламид – был разработан полвека назад. В 1954 году его начали использовать в качестве диуретического средства. В том же году была установлена способность ацетазоламида снижать ВГД у больных глаукомой.
Однако применение пероральных ИКА, таких как ацетазоламид и метазоламид, сопровождается побочными явлениями. Побочные эффекты включают симптомы недомогания, парестезии, желудочно–кишечные расстройства (тошнота, рвота и другие симптомы), потерю веса, депрессию, анорексию и потерю либидо. Также есть сведения о появлении лихорадки, сыпи (включая полиморфную эритему и синдром Стивенса–Джонсона), кристаллоурии, нарушений кроветворения, включая тромбоцитопению, гемолитическую анемию, лейкопению и агранулоцитоз [3, 6, 11].
Возникновение побочных эффектов системного характера ограничивает применение пероральных ингибиторов карбоангидразы для длительного лечения глаукомы. В основном они используются для лечения острого приступа глаукомы, купирования реактивного повышения ВГД после лазерных вмешательств или в течение короткого времени для подготовки больного перед антиглаукоматозной операцией.
Поэтому в течение многих лет исследователи пытались разработать местный ингибитор КА, чтобы избежать нежелательных системных проявлений. В 1986 г. впервые были опубликованы данные о возможном местном применении 10% раствора ацетазоламида. Экпериментальное исследование, проведенное у кроликов, показало, что инстилляции 10% раствора ацетазоламида снижают ВГД в среднем на 1,9–2,3 мм рт.ст. Однако прошло около 40 лет между демонстрацией гипотензивного эффекта перорального ацетазоламида в отношении ВГД и разработкой первых достаточно эффективных и безопасных местных ингибиторов КА. Трудности заключались в невозможности достичь достаточно высокой концентрации препарата, необходимой для значительного ингибирования КА цилиарного тела (для достижения фармакологического эффекта необходимо практически 100% подавление человеческой КА II, которая играет важную роль в секреции внутриглазной жидкости) [10, 11].
Разработка местных ингибиторов КА является значительным достижением в медикаментозном лечении глаукомы.
В настоящее время для больных доступны два ингибитора человеческой карбоангидразы местного применения. Данные препараты обладают хорошей биодоступностью, высокой селективностью и мощной ингибиторной активностью по отношению к изоферменту КА II. Обладая выраженным гипотензивным эффектом, они лишены побочных системных проявлений. К ним относятся 2% раствор дорзоламида гидрохлорида (Трусопт) – первый ингибитор карбоангидразы, предназначенный для местного лечения глаукомы, а также новый препарат – 1% офтальмологическая суспензия бринзоламида (Азопт) [3,11].
Местные ингибиторы КА, специфически подавляя КА II цилиарного тела, не оказывают других значимых фармакологических эффектов. Это объясняется тем, что терапевтическая доза и низкая системная абсорбционная способность этих препаратов не позволяют достичь уровня для системного угнетения КА. Низкий период их полувыведения из цилиарного тела обеспечивает пролонгированный гипотензивный эффект.
Чтобы оценить риск системного действия при длительном введении ИКА, было проведено исследование, в котором дорзоламид назначали внутрь здоровым добровольцам в дозе 4 мг/сут, что соответствует количеству активного препарата, проникающего в кровь при локальном применении 2% Трусопта 3 раза в день. Концентрации дорзоламида и его метаболитов в плазме крови были ниже минимального уровня, доступного для определения. Общая карбоангидразная активность в эритроцитах была подавлена на 81–88%, однако этот эффект был ниже уровня ингибирования (96%), который необходим для реализации действия препарата на функцию почек и дыхание. Сходные результаты были получены в клиническом исследовании Трусопта, который применяли 3 раза в день у 333 больных с повышенным ВГД [10].
По данным литературы, к наиболее частым побочным эффектам местных ингибиторов КА можно отнести жжение, зуд и покалывание в глазу, кратковременное затуманивание зрения или ощущение дискомфорта, следующее сразу за введением препарата. Некоторые пациенты отмечают изменение вкуса (горький, кислый или другое) после введения препарата. Были отмечены случаи поверхностного точечного кератита, блефарита, ринита.
Бринзоламид имеет более хорошую глазную переносимость, чем дорзоламид, что обеспечивается оптимальным составом суспензии и физиологическим pH. Степень глазной переносимости – важный показатель для больных, которые вынуждены применять препараты длительно. Многие исследования показывают, что различные проявления глазного дискомфорта после применения бринзоламида возникают примерно в 2 раза реже, чем при использовании дорзоламида. К тому же значительно больший процент пациентов вовсе не отмечают какого–либо глазного дискомфорта при применении бринзоламида в сравнении с дорзоламидом. [5,7,8].
Важно отметить, что, по данным ряда авторов, бринзоламид повышает кровоток в головке зрительного нерва у кроликов после местного применения [7,9].
Материал и методы
На I этапе исследования мы проводили сравнительную оценку гипотензивного эффекта и переносимости бринзоламида и дорзоламида. Процедура исследования на I этапе включала в себя биомикроскопию глаза (оценка состояния кожи и краев век, конъюнктивы, роговицы), исследование остроты зрения, измерение ВГД с помощью тонометра Гольдмана, пупиллометрию, офтальмоскопию. Оценка состояния проводилась до начала лечения и через 1, 2, 4, 6, 24 часа после инстилляции исследуемого препарата. Эффективность определялась выраженностью снижения ВГД от первоначального уровня.
Переносимость препарата оценивалась в соответствии со временем появления и выраженностью побочных реакций, их связи с применением исследуемого препарата. При оценке переносимости препарата регистрировались неприятные ощущения в глазу (чувство инородного тела, жжение и т.д.), аллергические проявления, изменения тканей глаза по данным биомикроскопии.
Исследование было проведено у 40 больных (20 здоровых добровольцев и 20 больных с некомпенсированной впервые выявленной ПОУГ в начальной стадии). ВГД измерялось после однократного закапывания исследуемых препаратов.
На II этапе проводилось изучение эффективности и безопасности длительного применения 1% офтальмологической суспензии бринзоламида два раза в день (в течение 3 месяцев), а также при применении бринзоламида три раза в день (в течение 1 месяца).
В 1–ю группу (бринзоламид дважды в день) были включены 30 больных (48 глаз) с некомпенсированной ПОУГ в начальной (44 глаза), развитой (2 глаза) и далекозашедшей стадии (2 глаза).
Во 2–ю группу (бринзоламид трижды в день) были включены 13 больных (20 глаз) с некомпенсированной ПОУГ в начальной стадии.
Ранее никто из больных медикаментозной гипотензивной терапии глаукомы не получал.
Всем больным до назначения лечения, а также еженедельно в течение 3 месяцев (для 2–й группы в течение 1–го месяца) проводилось обследование, которое включало биомикроскопию, офтальмоскопию, тонометрию по Гольдману (в 8 часов утра), измерение артериального давления и частоты сердечных сокращений.
Больным была назначена 1% офтальмологическая суспензия бринзоламида, которая применялась 2 раза в день (в 8 часов утра и 20 часов вечера в течение 3 месяцев для первой группы) и 3 раза в день (в 8, 14 и 20 часов в течение 1 месяца для второй группы). Другой местной и общей гипотензивной терапии не проводилось.
В ходе III этапа исследовалась возможность комбинированного применения 1% офтальмологической суспензии бринзоламида и 0,5% раствора тимолола малеата. Под нашим наблюдением находилось 20 больных (34 глаза) с впервые выявленной ПОУГ в начальной (24 глаза), развитой (8 глаз) и далекозашедшей (2 глаза) стадией. У всех отобранных для исследования больных отсутствовала компенсация ВГД после 2–х недельного применения 0,5% раствора тимолола малеата дважды в день.
Стандартное обследование и измерение ВГД по Гольдману проводилось в 8 часов утра до начала исследования, а также на 1, 2, 3 и 4 неделе. Всем больным дополнительно к назначенному ранее 0,5% раствору тимолола малеата (по 1 капле 2 раза в день) был назначен бринзоламид, который применялся 2 раза в день (в 8 часов утра и 8 часов вечера в течение 4 недель).
Результаты и обсуждение
На I этапе исследования при однократном применении бринзоламида у больных глаукомой снижение ВГД было более выражено по сравнению с группой здоровых пациентов, кроме того, у 2 здоровых добровольцев отмечалось повышение офтальмотонуса через 1, 2 и 6 часов после инстилляции препарата. Максимальное снижение ВГД отмечалось к 4 часу исследования в обоих группах. Динамика уровня ВГД была статистически достоверной (р > 95%) – см. табл. 1.
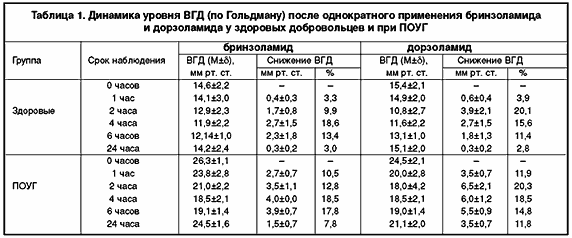
После однократного закапывания дорзоламида как у здоровых, так и у больных максимальное снижение ВГД соответствовало 2 часу исследования. В группе больных ПОУГ снижение ВГД было более выражено. Отмечалось сохранение гипотензивного эффекта через 24 часа. Динамика уровня была статистически достоверной (р > 95%), см. табл. 1.
После инстилляции дорзоламида 4 больных отмечали жжение в течение 5 минут.
При сравнении влияния исследуемых препаратов на офтальмотонус у больных с ПОУГ можно отметить, что оба препарата обладают выраженным гипотензивным эффектом (рис. 1). Большее снижение ВГД по сравнению с бринзоламидом после применения дорзоламида статистически недостоверно (p < 95%).
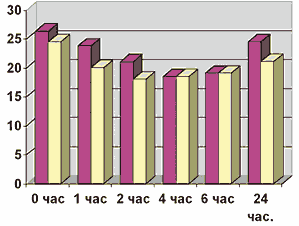
Рис. 1. Влияние исследуемых препаратов на офтальмотонус у больных с ПОУГ.
На II этапе проводилось исследование эффективности и безопасности бринзоламида при длительном применении. У больных в 1–й группе (бринзоламид дважды в день) до начала лечения уровень истинного ВГД составлял 26,0±2,6 мм рт. ст. Через 4, 8, 12 недель отмечалось снижение ВГД на 6,7 мм рт.ст. (25% от исходного уровня офтальмотонуса), 6,7 мм рт.ст. (26%) и на 7,2 мм рт.ст. (27%) соответственно.Во 2–й группе (бринзоламид 3 раза в день) начальное ВГД составляло 26,0±2,6 мм рт.ст. К концу 4–ой недели давление снизилось на 27% от первоначального уровня. Более наглядно еженедельную динамику ВГД на фоне применения исследуемого препарата в различных дозировках можно проследить на рис. 2. Изменение уровня ВГД было статистически достоверным (р > 95%).
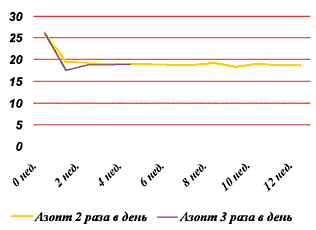
Рис. 2. Динамика ВГД (в мм рт. ст.) на фоне применения бринзоламида.
Из приведенных цифр видно, что имевшееся снижение ВГД после применения 1% бринзоламида 2 раза в день (в среднем на 7 мм рт.ст.) и 3 раза в день (на 7,6 мм рт.ст.) было статистически эквивалентно.В ходе III этапа изучалась возможность комбинированного использования 1% бринзоламида и 0,5% тимолола малеата. До начала лечения уровень истинного ВГД составлял 27,6±2,5 мм рт. ст. Через 2 недели на фоне применения 0,5% тимолола малеата отмечалось его снижение на 5,4 мм рт.ст, что составило 18,6% от исходного уровня. У 20 отобранных больных компенсация ВГД на данном этапе исследования отсутствовала: ВГД составляло 22,1±2,6 мм рт.ст.
В качестве дополнительной терапии был назначен бринзоламид. При совместном применении 2–х препаратов ВГД удалось снизить в среднем до 17,7±0,9 мм рт.ст. Более наглядно динамику ВГД на фоне применения исследуемых препаратов можно проследить с помощью табл. 2 и рис. 3. Изменение уровня ВГД было статистически достоверным (р > 95%).

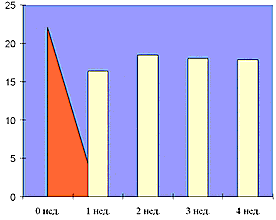
Рис. 3. Динамика ВГД при совместном применении 1% бринзоламида и 0,5% тимолола малеата.
На всех этапах исследования отмечалась хорошая местная и системная переносимость препарата. Среди побочных эффектов местного характера отмечались жжение, ощущение инородного тела в глазу и кратковременное затуманивание зрения, следовавшие сразу за введением препарата. Эти явления не требовали лечения и купировались самостоятельно через 5–10 мин после инстилляции. У 1 больной после однократного закапывания бринзоламида наблюдалась картина фибринозно–пластического иридоциклита, что потребовало отмены препарата и назначения стандартной противовоспалительной терапии в течение 4 дней.На протяжении всего срока лечения ни у одного из больных не было выявлено статистически значимого изменения частоты сердечных сокращений и уровня артериального давления. Не отмечалось никаких клинически значимых изменений общего состояния или параметров дыхательной деятельности. Во время исследования не выявлено существенных различий в остроте и поле зрения, состоянии переднего отрезка глаза, ширине зрачка и картине глазного дна.
Выводы
• Проведенное исследование показало, что бринзоламид оказывает выраженный гипотензивный эффект.
• Применение бринзоламида 2 раза в день позволяет контролировать уровень офтальмотонуса.
• Назначение бринзоламида 3 раза в день не сопровождается усилением гипотензивного эффекта.
• Бринзоламид не оказывает системного воздействия на организм и хорошо переносится больными.
• При комбинированном применении бринзоламида и тимолола малеата наблюдается аддитивный эффект.
1. Нестеров А.П. Глаукома. –М.:Медицина,1995.
2. Нестеров А.П.. Егоров Е.А. Медикаментозное гипотензивное лечение глаукомы. // Клиническая фармакология и терапия.–1994.–Т.3–№2.–с.86–88.
3. Егоров А.Е. Изучение гипотензивного действия и побочных эффектов ингибитора карбоангидразы дорзоламида гидрохлорида.// Вестник офтальмологии –1996–№2–с.3–4.
4. Либман Е.С., Шахова Е.В. Состояние слепоты и динамика слепоты и инвалидности вследствии патологии органа зрения в России. Тезисы докладов VII съезда офтальмологов России. Москва 16 – 20 мая 2000 г. с.209 – 215.
5. Silver L.H. Clinical efficacy and safety of brinzolamide (Azopt), a new topical carbonic anhydrase inhibitor for primary open–angle glaucoma and ocular hypertension. // Am–J–Ophthalmol. 1998 Sep; 126(3): 400–408.
6. Epstein, D.L., Grant, M.W.: Carbonic anhydrase inhibitor side effects. Arch. Ophthalmol. 95:1378–1382, 1977.
7. DeSantis L.: Preclinical Overview of Brinzolamide. Surv Ophthalmol 2000 Jan 1;44(4 Suppl 2):119–129.
8. Silver LH.: Ocular comfort of brinzolamide 1.0% ophthalmic suspension compared with dorzolamide 2.0% ophthalmic solution: results from two multicenter comfort studies. Brinzolamide Comfort Study Group. : Surv Ophthalmol 2000 Jan;44 Suppl 2:S141–5.
9. Barnes GE, Li B, Dean T, Chandler ML.: Increased optic nerve head blood flow after 1 week of twice daily topical brinzolamide treatment in Dutch–belted rabbits. Surv Ophthalmol 2000 Jan;44 Suppl 2:S131–40.
10. Sugrue MF.: Pharmacological and ocular hypotensive properties of topical carbonic anhydrase inhibitors. Prog Retin Eye Res 2000 Jan;19(1):87–112.
11. Bayer A.; Ferrari F.; Maren T.H.; Erb C. Topical carbonic anhydrase inhibitors in the treatment of glaucoma. // J–Fr–Ophtalmol. 1996; 19(5): 357–362.
